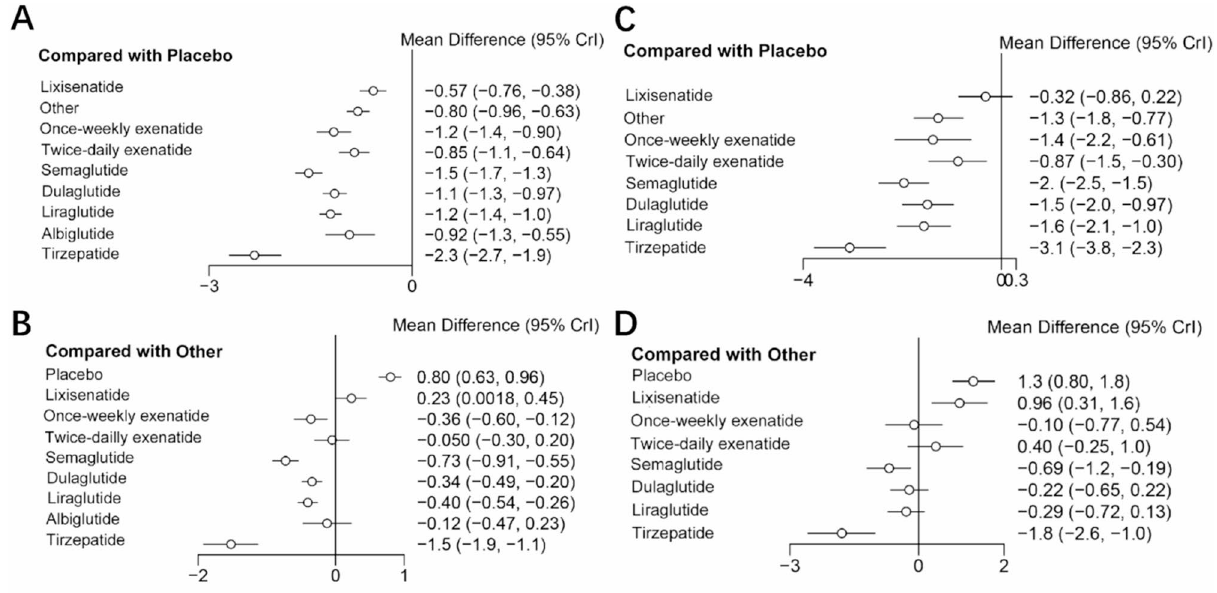
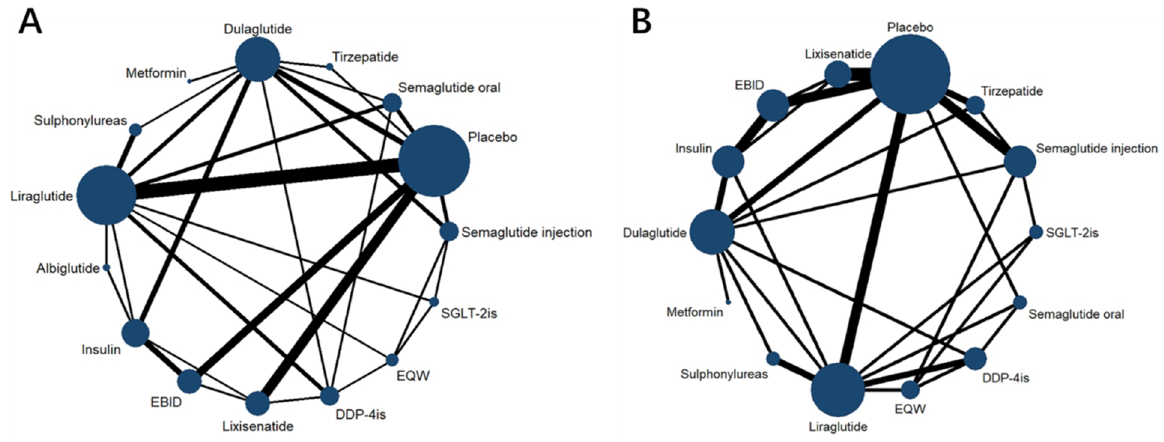
方法
PRISMA-NMA ガイドライン。PROSPERO登録番号: CRD42024595773.
文献検索および選定プロセス
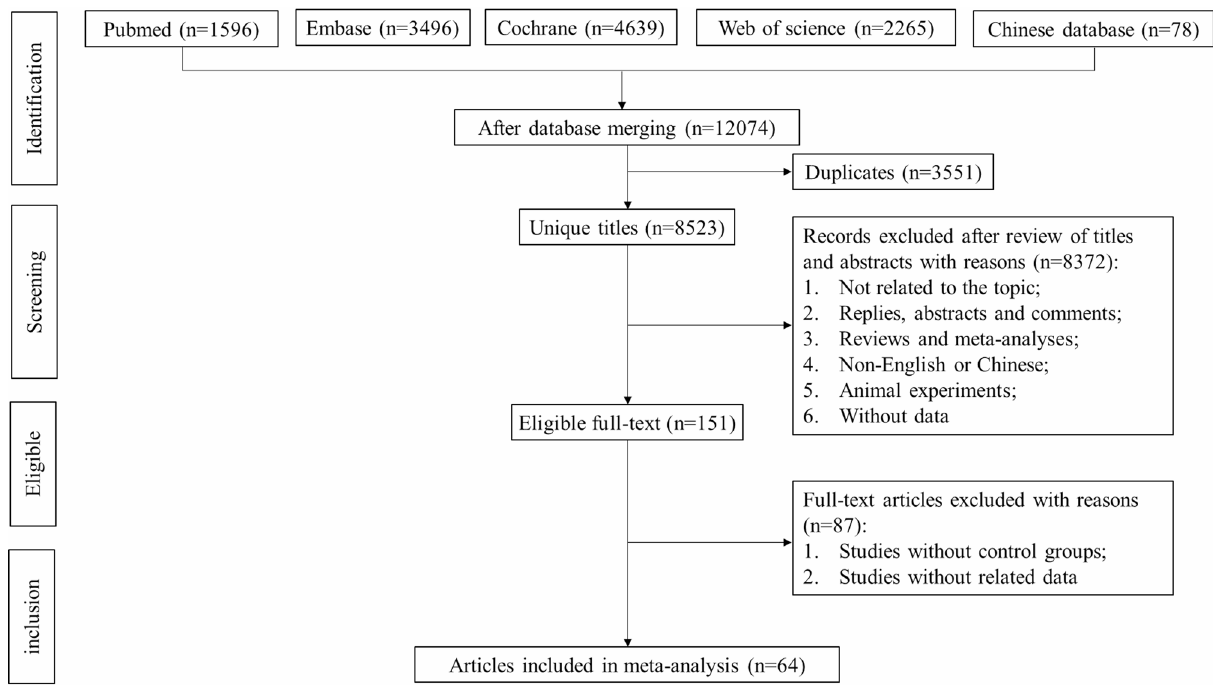
PRISMAフロー図:5つのデータベース全体で12,074件の記録を特定 → 最終的に64件のランダム化比較試験(RCT)が採用された。
データベース検索結果:PubMed (n=1,596) · Embase (n=3,496) · Cochrane (n=4,639) · Web of Science (n=2,265) · 中国のデータベース (n=78) → 重複を除去後:8,523件 → タイトル/抄録によるスクリーニング後:151件のフルテキストをレビュー → 最終的な採用:64件のRCT (25,572人の患者)
体系的な文献検索
2024年10月までに、PubMed、Cochrane Library、Embase、Web of Science、および中国のデータベース(CNKI、Wanfang)を検索しました。対象としたのは、並行群デザインのRCTのみです。2名の独立した評価者が、すべての論文のタイトル、抄録、および本文を評価しました。
無作為化比較試験(RCT)のみベイズネットワークを用いたメタ分析
NMA(ネットワークメタ分析)は、直接的な比較(直接的な対照試験)と間接的な比較(共通の比較対象を介した比較)の両方のエビデンスを統合し、直接比較されたことのない薬剤同士の比較を可能にします。SUCRA(累積ランキング曲線の面積)の値は、治療法を確率的にランク付けします。直接的なエビデンスと間接的なエビデンスとの整合性が評価されました。
解説:SUCRA(累積ランキング曲面積)とは?
NMA(ネットワークメタアナリシス)では、複数の薬剤を同時に比較するため、「どの薬剤が最も優れているか」を確率的に表す指標が必要です。SUCRA(Surface Under the Cumulative Ranking Curve)はその指標です。
直感的な理解:SUCRA = 「この薬剤が、すべての比較対象薬剤の中で最良である確率の期待値」(0〜100%)
- SUCRA 100%:ほぼ確実に最も効果的
- SUCRA 50%:中程度のランク
- SUCRA 0%:ほぼ確実に最も効果が低い
本研究におけるHbA1c低下でのSUCRA:チルゼパチド 97.6% → セマグルチド注射 87.2% → セマグルチド経口 79.4% → リラグルチド 65.1%。数値が大きいほど、「ランキングが高い確率が高い」薬剤です。
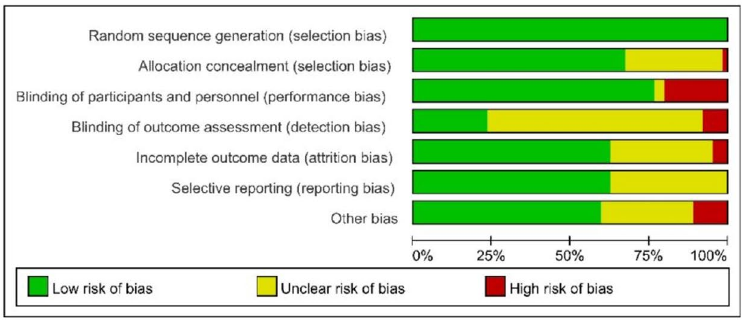
Cochrane リスク・オブ・バイアス評価
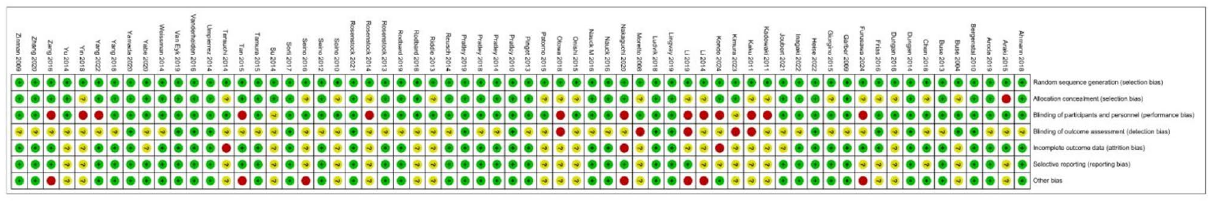
64件のRCT(ランダム化比較試験)について、2名の評価者がそれぞれ独立して評価を行い、Cochrane Risk of Bias (RoB) ツールを用いて、以下の7つの領域におけるバイアスを評価しました。具体的には、ランダムシーケンスの生成、割付の隠蔽、参加者および担当者のブラインディング、アウトカム評価のブラインディング、未完了のデータ、選択的報告、およびその他のバイアスです。
Cochrane RoB参加資格と結果.
対象となる研究は、成人(18歳以上)の確診された2型糖尿病患者を対象とした、並行群比較のランダム化比較試験であり、少なくとも1種類のGLP-1受容体作動薬(tirzepatide、semaglutide、liraglutide、dulaglutide、albiglutide、lixisenatide、exenatide QW、またはexenatide BID)と、プラセボまたは他の抗糖尿病薬(インスリン、メトホルミン、スルホニル尿素薬、DPP-4阻害薬、またはSGLT-2阻害薬)との比較を行ったものである。最小追跡期間は12週間であった。
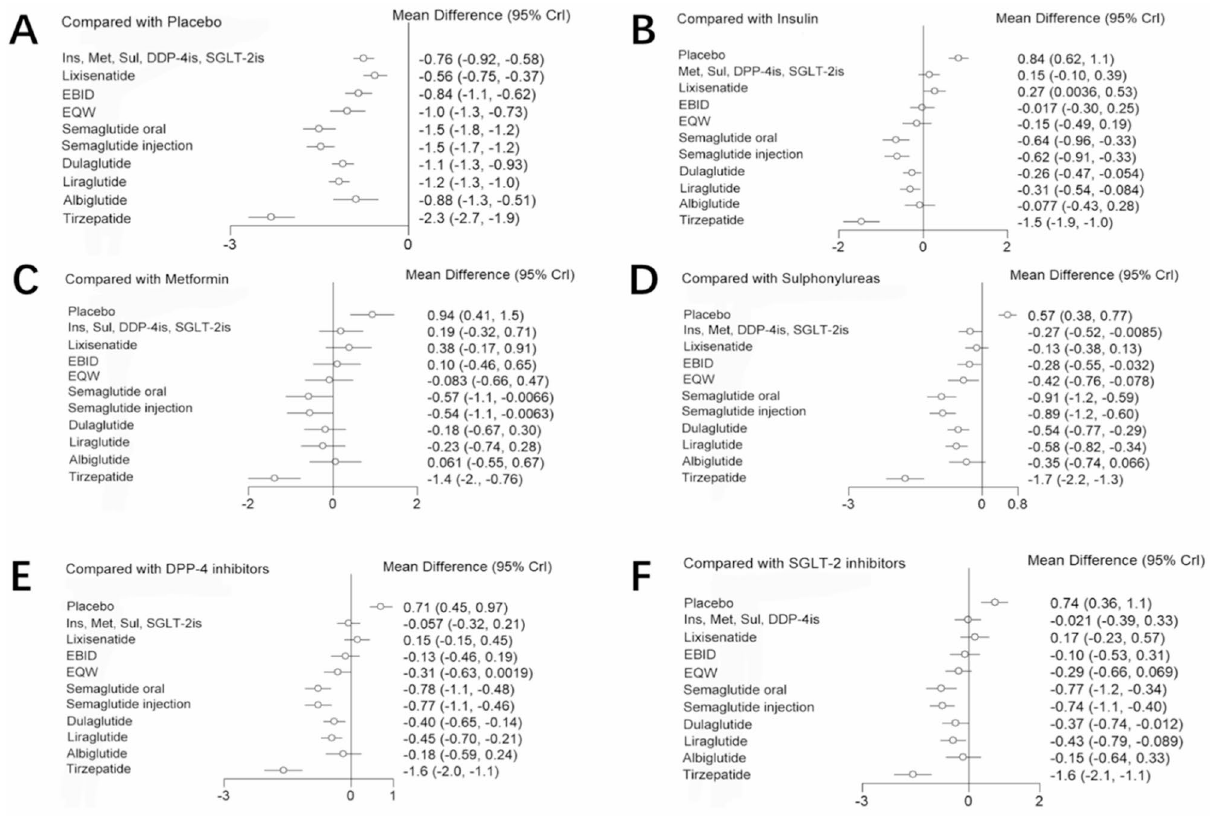
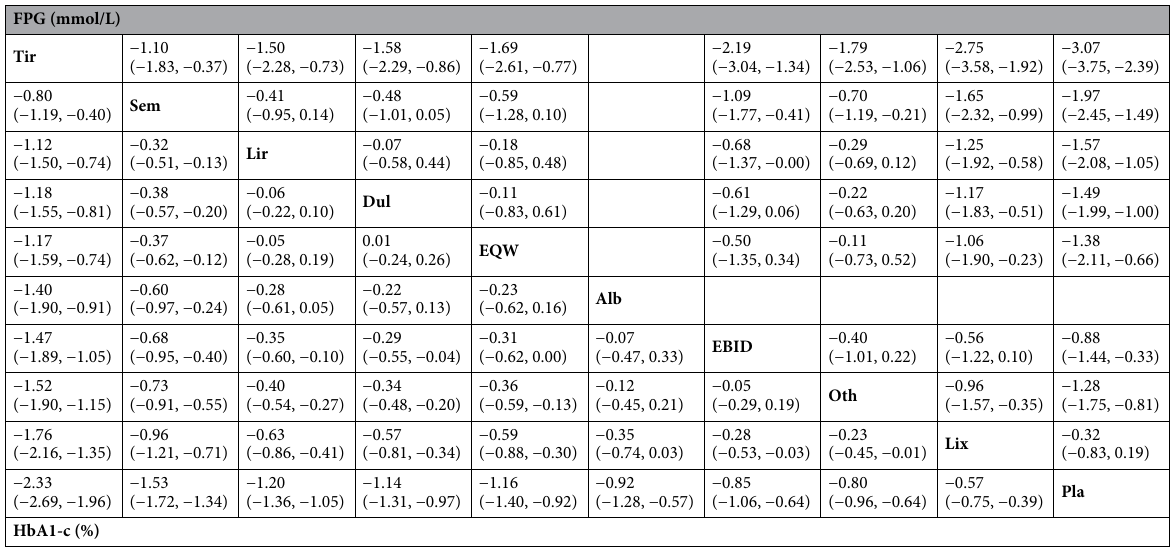
主要な評価項目は、ベースラインからのHbA1c(%)の変化と、空腹時血糖値(FPG、mmol/L)の変化です。副次的な評価項目には、体重(kg)、BMI(kg/m²)、収縮期血圧と拡張期血圧、総コレステロール(TC)、高密度リポタンパク質コレステロール(HDL-C)、低密度リポタンパク質コレステロール(LDL-C)、トリグリセリド、および安全性に関する評価項目(低血糖、吐き気、下痢、嘔吐、便秘、食欲不振など)が含まれます。
統計解析には、ベイズ法に基づくランダム効果メタアナリシスモデルが用いられました。異質性の評価には、I²統計量を使用しました。主要な結果の信頼性を検証するため、必要に応じて、セマグルチドの注射剤と経口製剤を、従来の薬剤クラスと統合した感度分析を実施しました。十分な数の研究があるアウトカムについては、漏洩バイアスの評価として、ファンネルプロットを使用しました。