グラフィカルな概要
Journal of Nanobiotechnology (2026) 24:142
肺疾患(喘息、肺がん、COPD、および肺線維症など)は、世界的な罹病率と死亡率の主要な要因であり、世界中の医療システムに大きな負担をかけています。RNAをベースとした治療法は、分子レベルで疾患を制御するための有望なツールとして登場していますが、効率的で肺特異的なRNAの送達を実現することは、臨床応用を制限する重要な課題です。
以前のレビューとは異なり、主にデリバリーシステムの性能指標をカタログとしてまとめているのに対し、このレビューは構造-機能設計の原則と臨床応用に関する知見を独自に統合しています。本レビューは、特定の物理化学的パラメータがどのように肺への移行性と治療効果を制御しているかというメカニズムを理解するための情報を提供します。
著者は、合成されたものと生物由来のもの両方のキャリアについて体系的に検討し、特に吸入、静脈内投与、および局所的な肺への投与を含む、肺を標的とした送達戦略に焦点を当てています。 彼らは、臨床試験の失敗(ALN-RSV01およびMRT-5005)から得られた教訓を批判的に分析し、主要な障壁を特定し、製剤の安定性、免疫学的適合性、およびスケールアップ可能な製造など、翻訳の展望について議論しています。

肺疾患(慢性閉塞性肺疾患(COPD)、喘息、特発性肺線維症(IPF)、肺癌など)は、世界的な罹病率および死亡率の主要な原因であり、患者の生活の質に深刻な影響を与えます。これらの疾患は、遺伝的な感受性、環境汚染物質、および微生物病原体といった複雑な多因子的な相互作用によって引き起こされ、疾患の多様な現れ方をもたらし、治療介入を困難にしています。COVID-19パンデミックは、呼吸器系の脆弱性を浮き彫りにし、既存の治療法の重要な欠点を明らかにした。
従来の治療法は、主に症状の緩和に重点を置いており、疾患の根本原因に対処するものではありません。そのため、長期的な効果が制限されることがあります。RNAをベースとした治療法」には、アンチセンスオリゴヌクレオチド(ASOs)、siRNA(small interfering RNAs)、circRNA(circular RNA)、およびmRNA(messenger RNAs)などがあり、これらは遺伝子発現を調節することで、機能性タンパク質の再発現を促したり、病原性タンパク質の合成を分子レベルで抑制したりするという、根本的に異なるアプローチを提供します。
翻訳されたmRNAは、ホストのリボソームによって翻訳され、機能的なタンパク質を生成します。これにより、タンパク質置換療法、ワクチン、およびゲノム編集といった応用が可能になります。COVID-19 mRNAワクチンは、この技術の変革的な可能性を示しました。
二重鎖RNA二重鎖構造体が、RNA誘導性サイレンシング複合体 (RISC)に組み込まれ、標的mRNAの配列特異的な切断を誘導します。これにより、疾患を引き起こすタンパク質に対する強力な遺伝子サイレンシングが実現されます。
遺伝子発現を転写後で制御する、比較的小さな非コードRNA。複数の遺伝子を同時に調節することができ、多因子経路を持つ複雑な疾患に対する治療的可能性を秘めています。
一本鎖で、化学的に修飾されたオリゴヌクレオチドであり、相補的なRNA標的にハイブリダイズします。 RNase H1を介した分解、翻訳の立体障害、または前mRNAのスプライシングの調節によって、遺伝子発現を抑制します。
呼吸器系へのRNAの効率的な送達には、複数の連続する生物学的バリアを克服する必要があり、それぞれのバリアが特有の課題を提示し、それらが総合的に治療効果を決定します。
まるで、多層のセキュリティシステムを通過させる荷物を送ろうとしているようなものです。肺は、異物を排除するための高度な防御機構を進化させてきました。これには、侵入者を捕らえる粘着性の粘液層、異物を払い落とす微細な毛のような繊毛、不審なものを食べる免疫細胞(肺胞マクロファージ)、そして、RNA分子を特異的に破壊する酵素(RNases)などが含まれます。治療用のRNAナノ粒子が効果を発揮するためには、これらのすべての障壁を乗り越え、そして、細胞内に侵入した後、消化される前に酸性のエンドソーム区画から脱出しなければなりません。現在、ナノ粒子のうち、最終的な脱出段階を達成できるのは、わずか2%未満です。
| NCT Number | Disease | Product (Sponsor) | Route | Phase | Carrier |
|---|---|---|---|---|---|
| NCT06747858 | Cystic Fibrosis | ARCT-032 (Arcturus) | Inhaled | Phase 2 | LNP |
| NCT05668741 | Cystic Fibrosis | VX-522 (Vertex) | Inhaled | Phase 1/2 | LNP |
| NCT05660408 | Cystic Fibrosis | RCT1100 (ReCode) | Intravenous | Phase 1/2 | LNP |
| NCT03375047 | Cystic Fibrosis | MRT5005 (Translate Bio) | Inhaled (nebulized) | Phase 1/2 | LNP |
| NCT06928922 | Respiratory Infection | Inhaled mRNA vaccine | Inhaled (dry powder) | Phase 1 | LNP dry powder |
| NCT03946800 | Solid Tumors (incl. NSCLC) | Intratumoral mRNA vaccine | Intratumoral | Phase 1 | LNP |
| NCT03819387 | NSCLC | NBF-006 (Nitto BioPharma) | Intravenous | Phase 1 | LNP |
| NCT05677893 | COVID-19 | MBS-COV (Oneness Biotech) | Inhaled | Phase 1 | Modified |
| NCT04504669 | NSCLC | AZD8701 (AstraZeneca) | Intravenous | Phase 1 | Modified |
この吸入型siRNAは、RSVのヌクレオカプシドタンパク質を標的とし、第II相試験において優れた忍容性を示しました。しかし、プラセボと比較して、有意な抗ウイルス効果を示すことができなかった. 後見的な分析の結果、感染した上皮細胞への十分なsiRNAの送達が不足しており、また、急速な粘液毛輸送が、効果的な標的への作用を阻害していることが明らかになりました。重要な教訓: 忍容性だけでは不十分であり、標的細胞集団への送達効率が最も重要です。
このネブライザー送達型mRNAは、嚢胞性線維症の治療に用いられ、機能性CFTRタンパク質をコードしており、第I/II相の臨床試験において、投与量依存的なppFEV1の増加が確認されました。しかし、その後の分析により、ネブライザー条件下での製剤の不安定性、患者間でのCFTR発現レベルの不均一性、および反復投与における課題が明らかになりました。重要な教訓: 実際の投与条件下(エアロゾル化によるストレス、温度など)での製剤の安定性は、臨床的な成功に不可欠です。
様々な肺疾患は、それぞれ特有の生物学的障壁、標的細胞集団、そして送達における課題を提示します。これらの疾患特有の要因を理解することは、合理的なキャリア設計と治療戦略の選択にとって不可欠です。
| Disease | Primary Target Cells | Key Pathological Barriers | RNA Therapeutic Targets | Delivery Challenges |
|---|---|---|---|---|
| Cystic Fibrosis | Airway epithelial cells | Thick dehydrated mucus; impaired mucociliary clearance | CFTR (mRNA replacement); ENaC (siRNA knockdown) | Mucus penetration; repeated dosing requirement |
| COPD | Epithelial cells; alveolar macrophages | Mucus hypersecretion; chronic inflammation; emphysematous changes | Inflammatory mediators (TNF-α, IL-1β); protease inhibitors | Heterogeneous disease; variable lung architecture |
| Pulmonary Fibrosis | Fibroblasts; myofibroblasts; AT2 cells | Excessive ECM; altered epithelial integrity; honeycombing | TGF-β; HSP47; collagen genes | Access to fibrotic regions; targeting activated fibroblasts |
| Lung Cancer | Tumor cells; cancer stem cells; immune cells | Dense stroma; heterogeneous receptor expression; immunosuppressive TME | Oncogenes (KRAS, EGFR); tumor suppressors (p53); immune checkpoints | Tumor penetration; specificity; systemic toxicity |
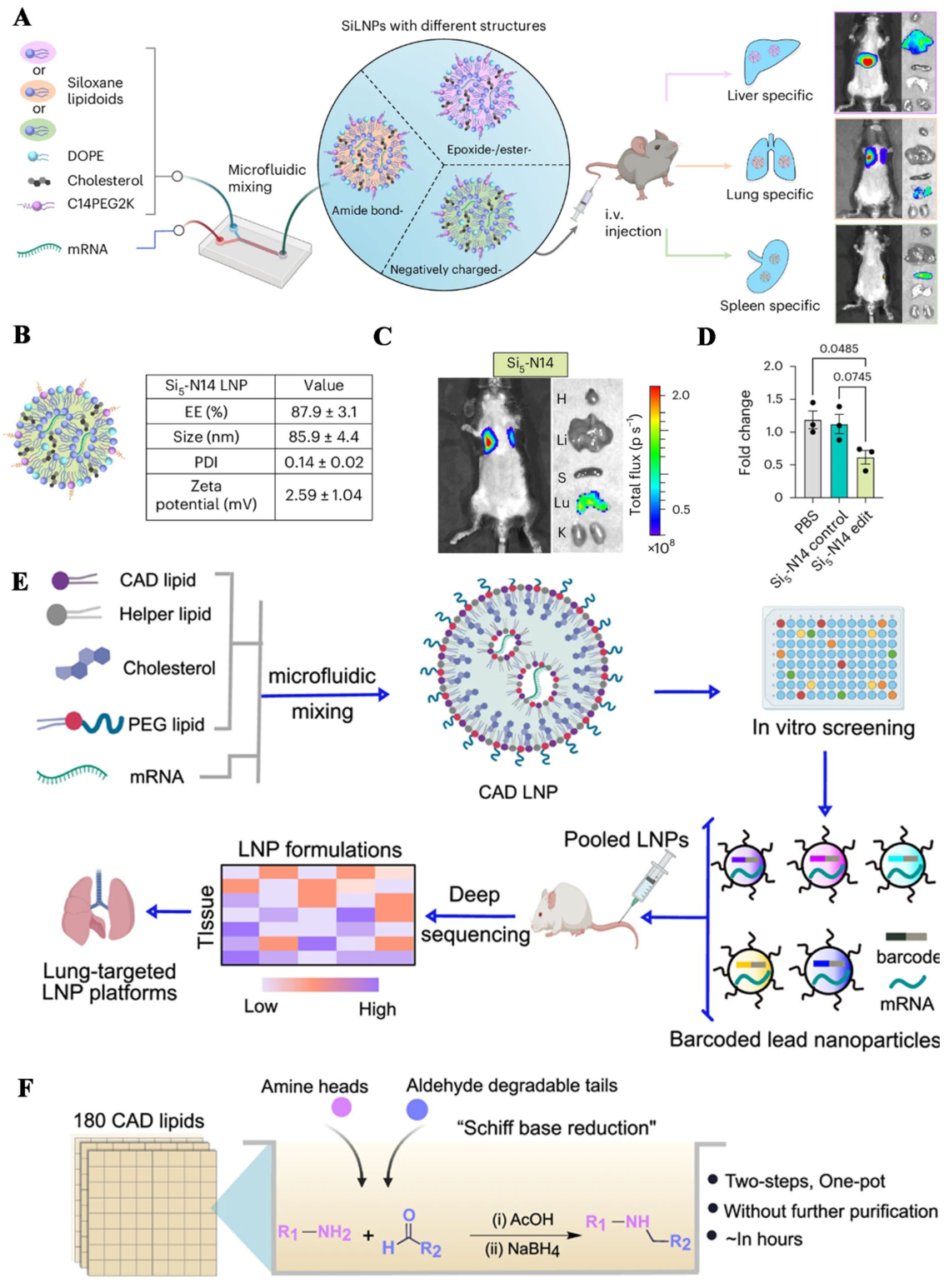
LNPは、非常に小さな脂肪ベースの微粒子(通常は50~200 nm—人間の髪の毛の幅の約1/500)で、RNA分子を包み込み、細胞への送達を保護する役割を果たします。もしあなたが、PfizerまたはModernaからCOVID-19のmRNAワクチンを受けたことがあるなら、すでにLNP技術の恩恵を受けています。各LNPには、主に以下の4つの成分が含まれています。
LNPsは、RNAデリバリーのための最も臨床的に検証されたプラットフォームであり、COVID-19 mRNAワクチンの成功は、規制および製造に関する先例を確立しました。典型的なLNPは、以下の4つの構成要素を含みます。イオン化可能脂質(RNAの封入とエンドソームからの脱出のため)、補助脂質(構造的安定性)、コレステロール(膜の剛性)、およびPEG-脂質(立体的な安定化と持続的な循環)。
次世代のイオン化可能脂質が、臓器選択的な送達においてパラダイムシフトをもたらしています。SORT(Selective Organ Targeting)技術は、DOTAPのような常に帯電した脂質を、定義されたモル比(10~50%)で組み込み、静脈内投与後に肺への優先的な蓄積を達成します。このトロピズムの変化は、タンパク質コロナの組成の変化と相関しており、具体的には、肺内皮への取り込みを誘導するビトロネクチンやインテグリン結合タンパク質の増加が挙げられます。
ハイスループットのコンビナトリアルスクリーニングは、LNP(脂質ナノ粒子)の最適化を加速させています。研究者たちは、バーコードでラベル付けされたLNPライブラリ(100種類以上のユニークな脂質製剤を含む)を開発しました。これらのライブラリをプールして単一の動物に投与し、臓器特異的なバーコード分布を深層シーケンシングで解析することで、肺への移行性が高い候補物質を特定することができます。CAD(Combinatorial Aldehyde Degradable)脂質ライブラリのアプローチでは、シッフ塩基還元反応によって180種類の脂質が合成されました。
肺に特有の課題に対して、吸入式ドライパウダー型LNP製剤は、ネブライゼーションと比較して、LNPの構造的完全性を損なうせん断力を回避できるという利点があります。PLGA修飾されたLNPは、肺組織において、安定性と持続的な放出特性の向上が確認されています。LNPのプラットフォームとしての性質により、イオン化可能な脂質、ターゲティングリガンド、およびRNAペイロードを、様々な疾患に対してモジュール的に交換することができます。
アクティブなターゲティング戦略には、肺に特異的な抗体、ペプチド、またはアプタマーとの結合が含まれます。リガンドを使用しないアプローチは、内因性のタンパク質コロナを利用して、臓器選択性を実現します。 「PEGジレンマ」は依然として重要な課題です。PEG化は循環時間を改善しますが、細胞内への取り込みを低下させ、繰り返しの投与によって抗-PEG免疫応答を引き起こす可能性があります。
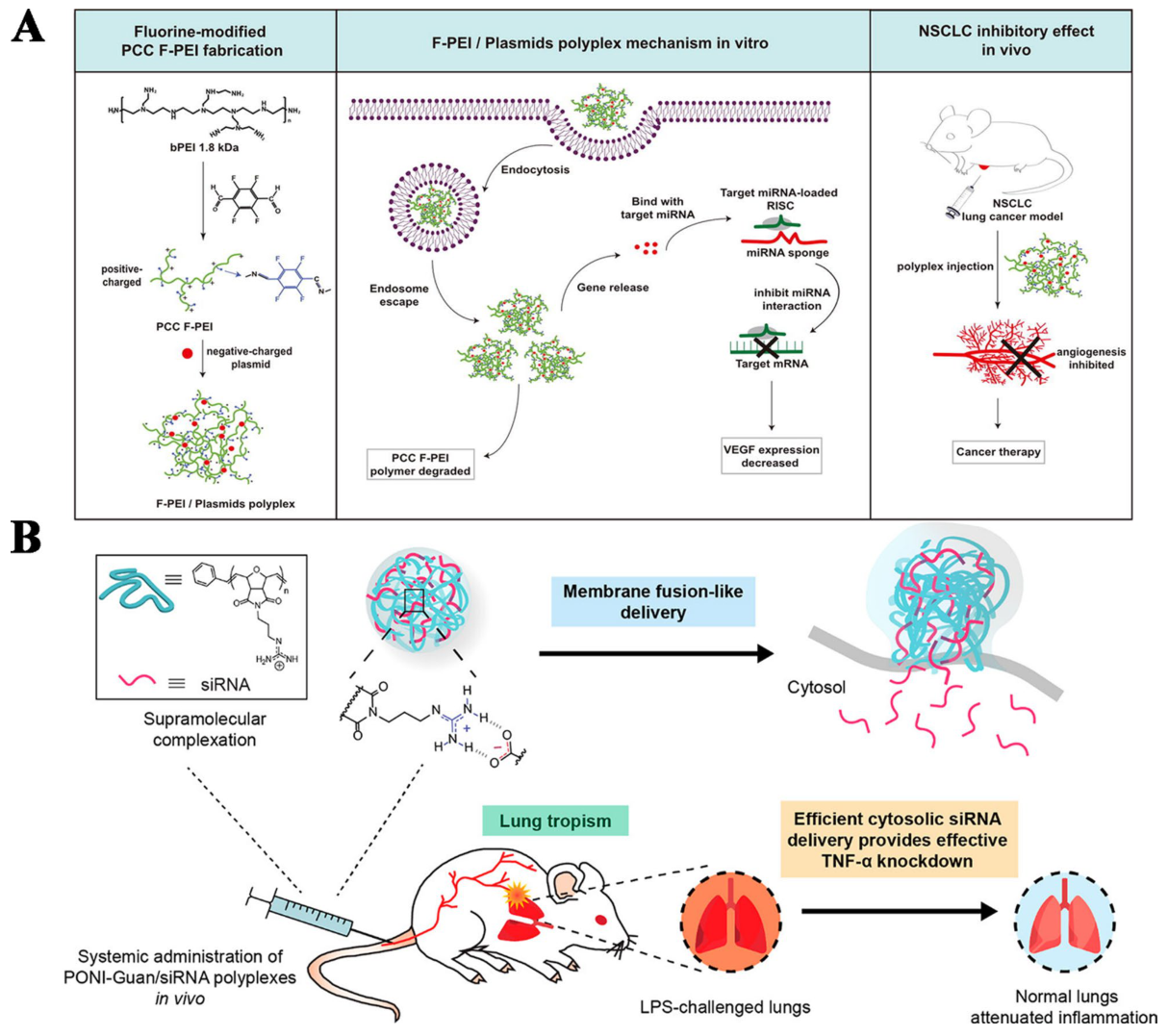
RNA送達のためのポリマーキャリアには、いくつかの種類があります。カチオン性ポリマー(例:PEI、PBAE)は、負電荷を持つRNAと静電的に複合体を形成し、生分解性ポリマー(例:PLGA、キトサン)は、徐放性を実現し、デンドリマー(例:PAMAM)は、多価RNA結合のための明確な分岐構造を持っています。
RNA複合体の形成メカニズムは、正に帯電したポリマーと負に帯電したRNAの主鎖との間の静電的相互作用に基づき、凝縮したポリプレックスを形成します。細胞内への送達は、特にエンドソームからの脱出に依存しており、これはしばしば「プロトンスポンジ効果」によって達成されます。この効果とは、アミン基の緩衝能が浸透圧の膨張を引き起こし、エンドソーム膜が破裂する現象を指します。
フッ素修飾されたPEI(F-PEI)ポリプレックスは、非小細胞肺癌(NSCLC)の治療において、効果的なmiRNAの送達能を示し、miRNAスポンジとして機能し、VEGFの発現を抑制し、腫瘍血管新生を抑制します。PONI-Guan/siRNAポリプレックスは、膜融合のような送達メカニズムにより、肺への選択的な送達を達成し、細胞質への効率的なsiRNAの送達を可能にし、LPSで刺激された肺におけるTNF-αの抑制を実現します。
ポリマーキャリアの主な制限事項には、細胞毒性(特に高分子量のPEIの場合)、バッチごとのばらつき、および変動するトランスフェクション効率が含まれます。 解決策としては、フッ素化、PEG化、生分解性リンカーの設計、および制御された分子量最適化などが挙げられます。
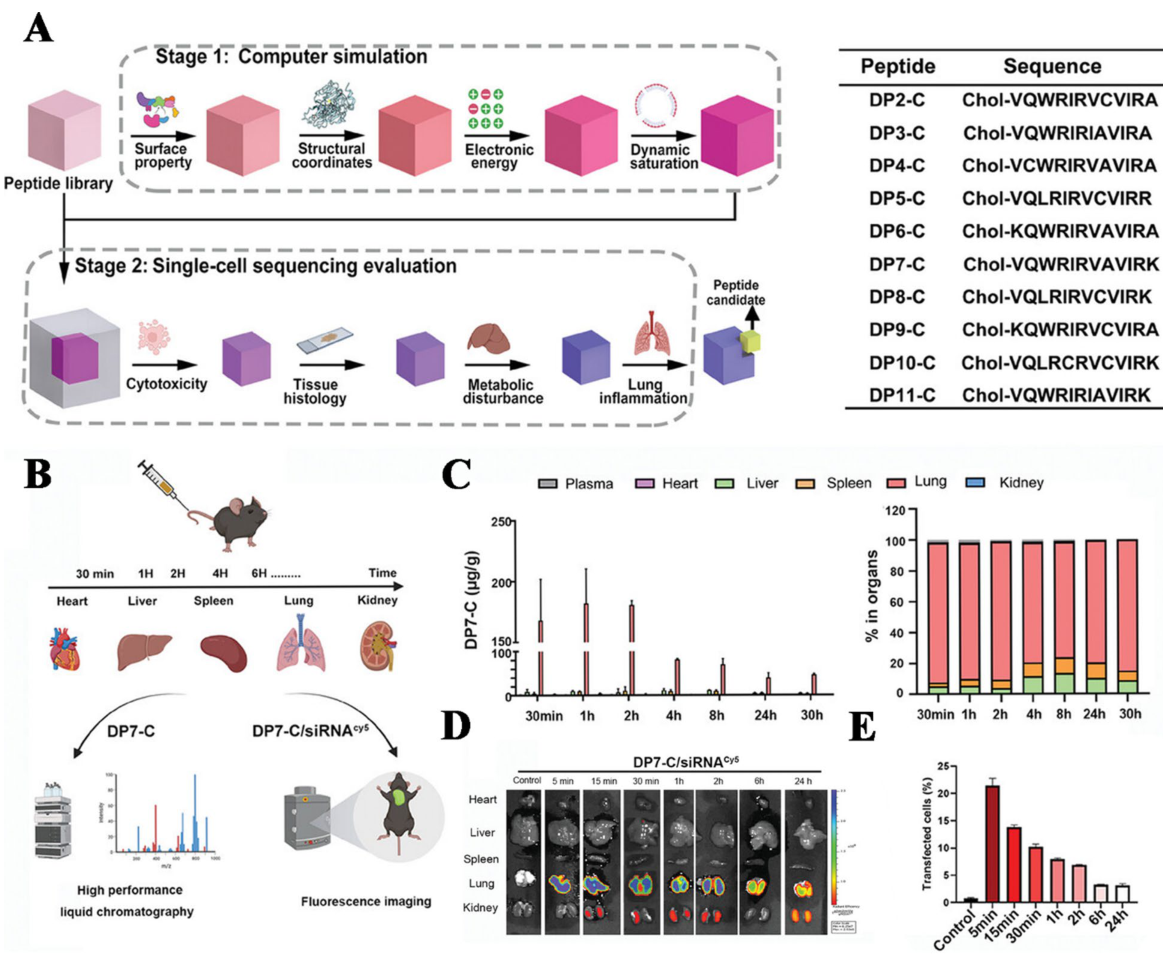
ペプチドベースのベクターは、細胞透過性ペプチド(CPPs)、両親媒性ヘリカル構造、およびコレステロール結合を利用して、細胞内への取り込みとエンドソームからの脱出を実現します。計算アプローチ—分子動力学シミュレーションや機械学習など—は、肺へのターゲティングに最適化されたペプチドライブラリの合理的な設計を可能にします。
DP7-Cペプチド(コレステロール結合したVQWRIRVAVIRK配列)は、コンピュータシミュレーションとシングルセルシーケンシング評価を組み合わせた二段階のスクリーニングパイプラインによって同定されました。このペプチドは、肺への選択的な蓄積と、生体内での効果的なsiRNA送達を示し、細胞毒性、組織学的検査、代謝評価において良好な安全性プロファイルを有していました。
ペプチドベクターは、精密なターゲティングと生体適合性において利点があるものの、急速な酵素分解、限られたペイロード容量、そしてLNPと比較して低いトランスフェクション効率といった課題に直面しています。D-アミノ酸の置換、環化、PEG化などの戦略は、安定性と薬物動態を改善することができます。
ウイルスベクターは、生物学的に進化してきた送達システムであり、細胞への侵入や遺伝子発現のために、天然のウイルス機構を利用します。肺へのRNA送達に使用される主要なタイプは4つあり、それぞれに独自の利点と欠点があります。
ウイルスは、自然界で最も効率的な遺伝子送達システムです。何億年もの進化の過程で、ウイルスは自身の遺伝物質を細胞内に送り込む能力を獲得しました。科学者たちは、病気を引き起こす遺伝子を除去し、代わりに治療効果のあるRNAを組み込むことで、ウイルスを再利用することができます。しかし、トレードオフとして、私たちの免疫システムもまた、ウイルスを認識し、攻撃する能力を進化させてきました。これが、ウイルスベクターの効果を制限する可能性があります(特に、繰り返し投与する場合)。非ウイルスベクターであるリポソーム(LNPs)やエクソソームは、同様の強い免疫反応を引き起こしにくいですが、一般的に細胞内への侵入効率は低くなります。理想的な送達システムは、治療対象となる特定の疾患によって異なります。
利点: 高い感染効率、大きな搭載容量(ヘルパー依存型の場合、約36 kb)、確立された生物学的特性。 欠点: 強い免疫原性、一時的な発現、多くの患者において既存の免疫が存在する。 ヘルパー依存性アデノウイルス(HDAd)は、全てのウイルス由来の遺伝子配列を除去することで免疫原性を低減します。
長所: 長期的な発現を可能にする安定したゲノムへの組み込み、細胞分裂していない細胞への導入能力、制御されたプロモーターシステム(テトラサイクリン誘導性)。 短所: 挿入変異のリスク、複雑な製造プロセス、擬似型化なしでは肺への移行能力が限定的。 好気性マクロファージの導入に有効です。
利点: 低免疫原性、組み込みなしでの長期的な発現、異なる組織への作用を持つ複数の血清型(肺への作用を持つAAV5、AAV6、AAV9)。CRISPR/Cas9の送達は、NIH SCGEプロジェクトで実証済み。 欠点: 搭載できる遺伝子量(約4.7 kb)が小さい、既存の中和抗体、製造の複雑さ。
利点: 遺伝子改変を恒久的に行うための安定した統合が可能であり、確立された技術です。 欠点: 分裂している細胞のみに導入可能であるため、肺への応用が制限されます。また、挿入変異のリスクがあり、肺への送達においては他のウイルスベクターと比較して効率が低い場合があります。
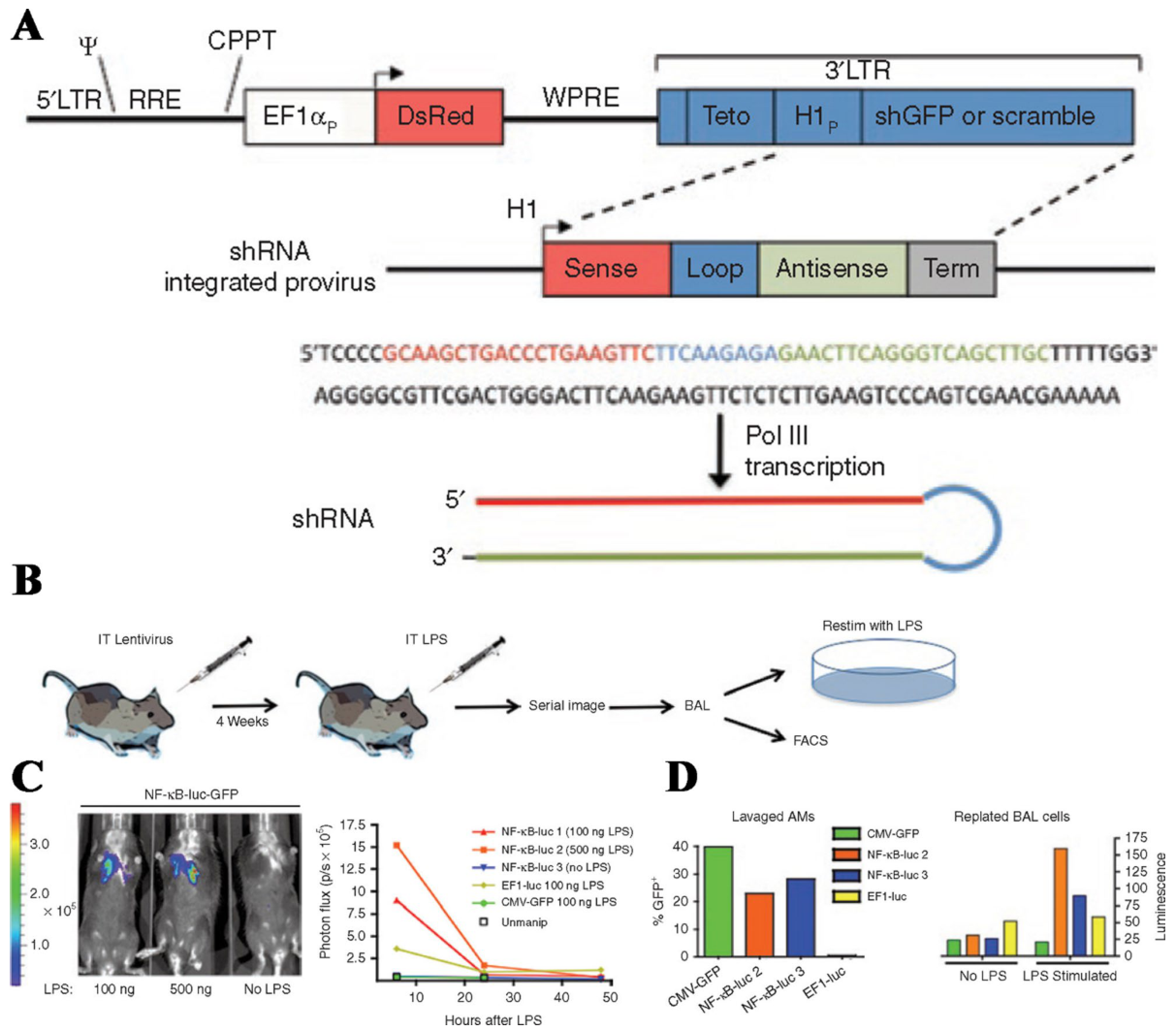
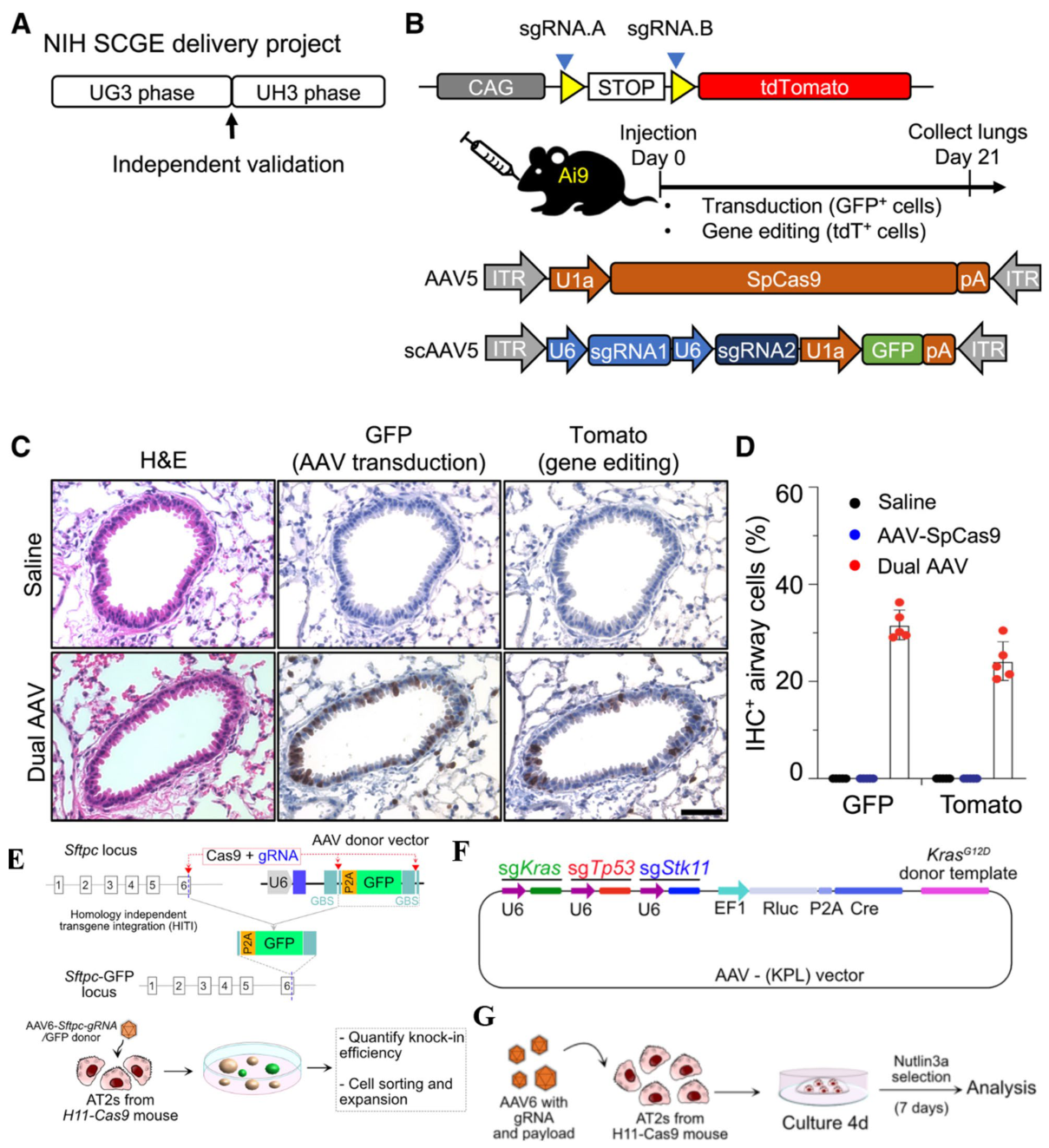
エクソソームは、天然由来の細胞からの細胞外小胞(30~150 nm)であり、RNAの送達において、生体適合性と低い免疫原性という利点があります。表面改変技術により、標的指向性の送達が可能になります。例えば、EGFRvIII抗体フラグメントでエクソソームを修飾することで、EGFRを過剰発現する腫瘍へエクソソームを誘導することができます。ペイロードを積載する方法としては、電気穿孔法、超音波処理法、およびインキュベーション法などがあります。
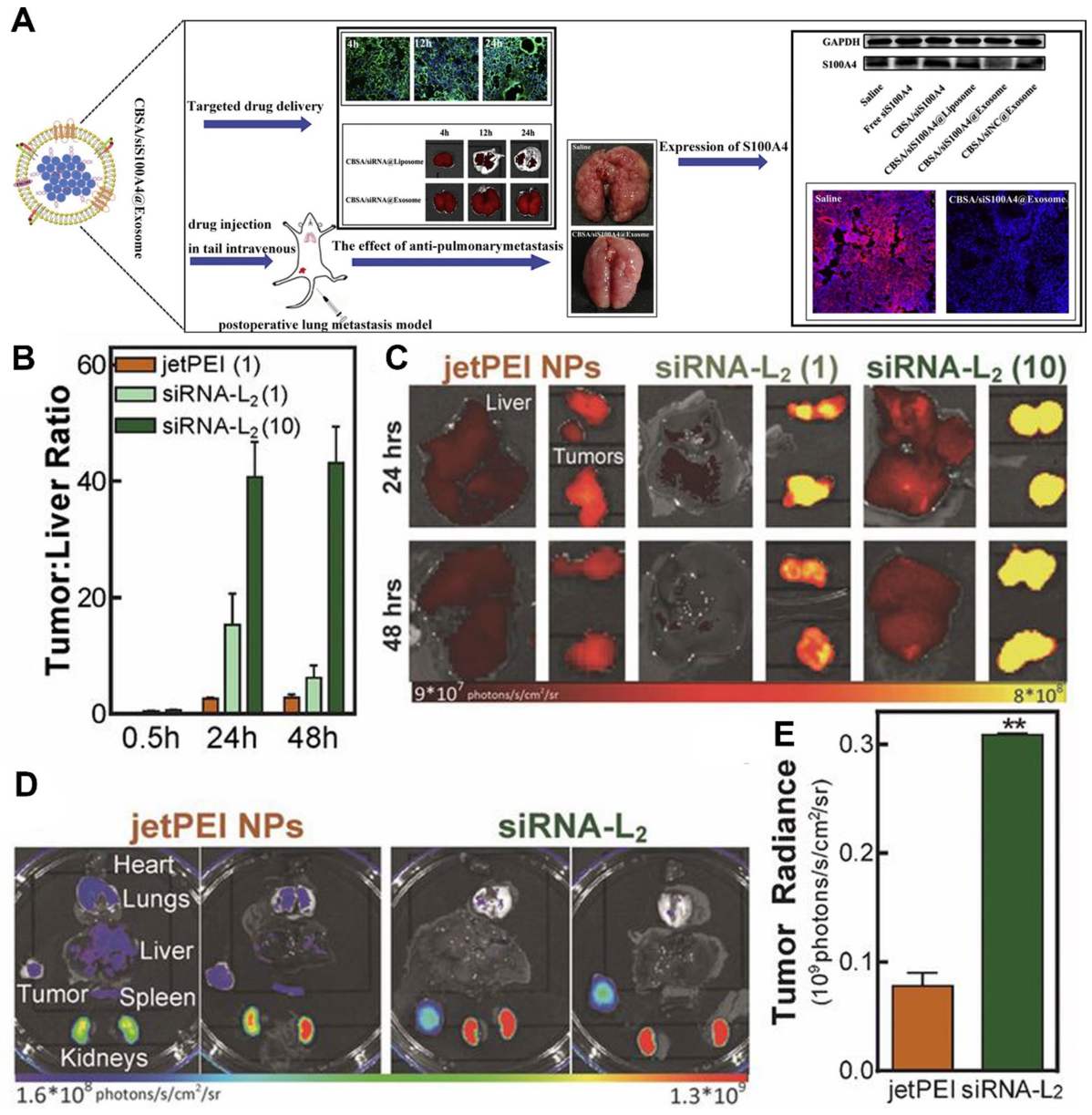
主な利点には、生物学的バリアを透過する自然な能力、細胞間のコミュニケーション能力、および血液脳関門を通過する可能性が含まれます。しかし、大規模な製造、バッチ間の変動、合成システムと比較して相対的に低いRNA搭載効率、および表面修飾中のベシクル構造の維持の難しさといった課題が残されています。CRISPR/Cas9で修飾されたエクソソームは、抗転移療法において有望な結果を示しています。
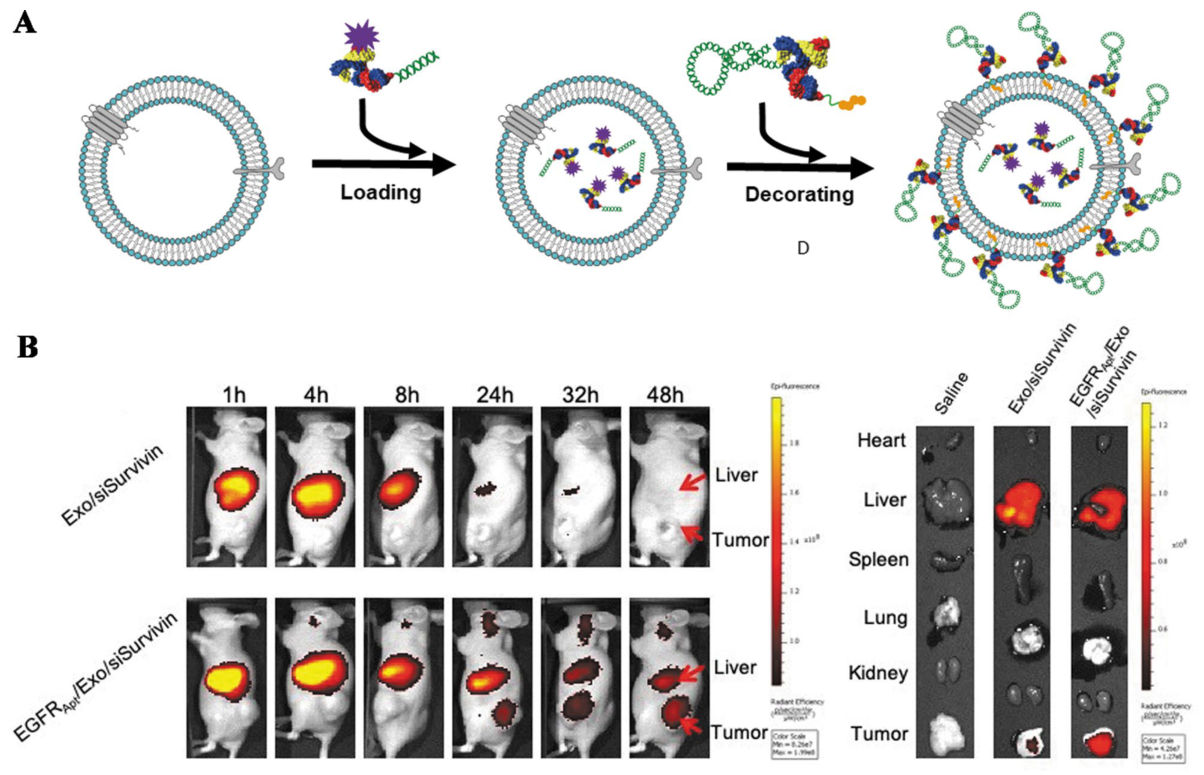
タンパク質キャリアは、RNAを封入し、標的デリバリーを行うために、天然のタンパク質構造を利用します。アルブミンをベースとしたシステムは、最も豊富な血清タンパク質(HSA)を利用して、生体適合性に優れたナノ粒子を生成します。CTX-HSAナノ粒子とTGF-β-1 siRNA LNPを組み合わせることで、肺癌に対する併用療法が可能となり、腫瘍への標的薬物送達と遺伝子サイレンシングを同時に実現します。
フェリチンナノケージは、自己組織化するタンパク質シェル(~12 nm)であり、その中空部分にRNAを封入することができます。その表面は、遺伝子または化学的な修飾によって標的化に適しています。トランスフェリン受容体標的型タンパク質-ポリマーハイブリッドは、トランスフェリンの結合特異性とポリマー成分の搭載能力を組み合わせたものです。
新たな技術には、非ウイルス由来のタンパク質カプシドを利用したものが含まれており、これはウイルスに似た細胞への取り込みメカニズムを提供しつつ、ウイルスベクターに伴う免疫原性の問題を回避できるという利点があります。これらのシステムは、生物学的および合成的な設計原則の有望な融合を示しています。
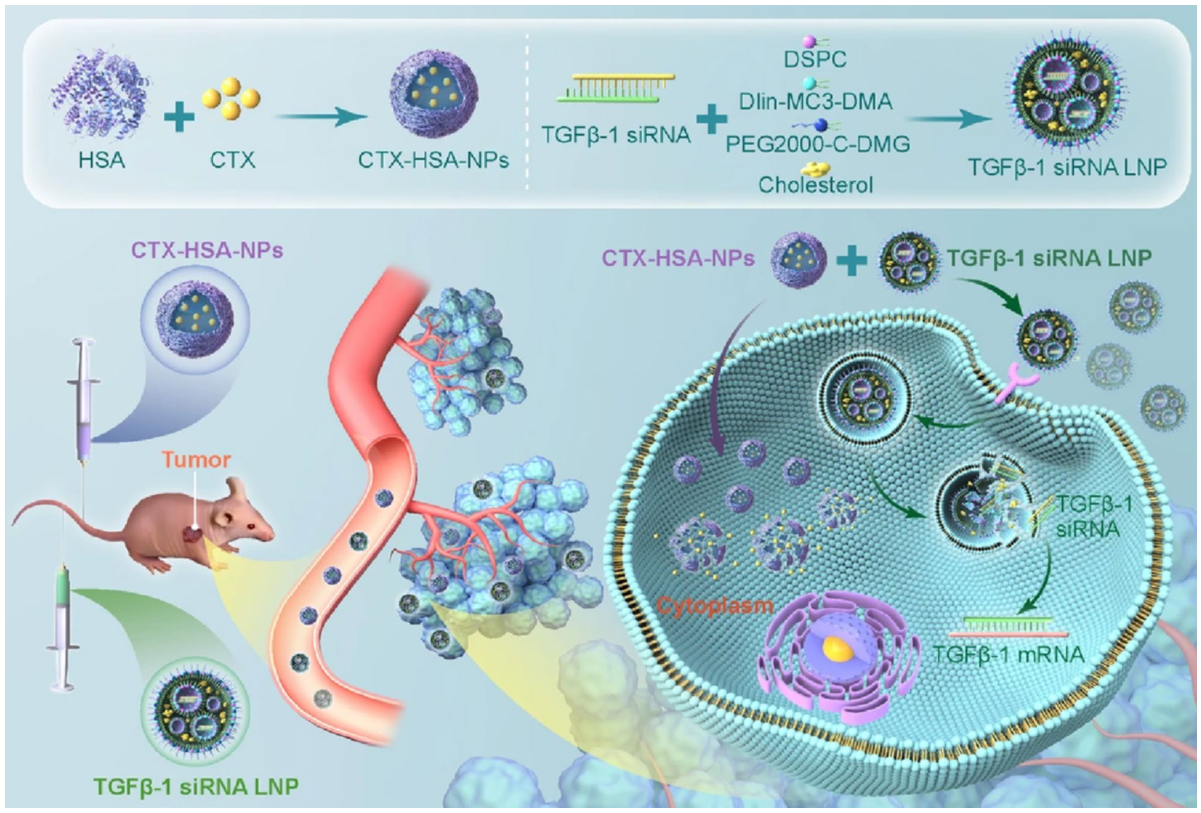
比較分析は、普遍的に最適なキャリアを特定するのではなく、状況に応じたアプローチによるデリバリープラットフォームの選択を支持しています。各プラットフォームのカテゴリには、特定の臨床シナリオと一致する独自の強みがあります。
強み: スケーラブルなGMP製造、調整可能な物理化学的特性、規制上の先行事例(COVID-19ワクチン)、モジュール式のプラットフォーム設計。 制限事項: 用量依存性毒性、反復投与によるPEGに対する免疫反応、エンドソームからの脱出効率が2%未満。 最適な用途: 一時的な高レベルのタンパク質発現を必要とする急性介入、ワクチン、確立された疾患ターゲット。
長所: 生体適合性、細胞への取り込みメカニズムの進化、長期間の遺伝子発現(ウイルス)、バリアを通過する能力(エクソソーム)。短所: 製造のスケールアップ、ロット間のばらつき、既存の免疫反応(ウイルス)、低い搭載効率(エクソソーム)。最適な用途: 永続的な修正が必要な遺伝性疾患、自然なターゲティングが有利な疾患。
長所: 高いターゲティング精度、生体適合性、合理的な計算設計、モジュール式の表面化学。 制限事項: 迅速な酵素による分解、限られたペイロード容量、低いトランスフェクション効率、安定性の課題。 最適な用途: 特定の肺細胞集団への精密ターゲティング、他のキャリアとの組み合わせ戦略。
RNA送達プラットフォームの選択は、荷物を送るための輸送方法を選ぶのに似ています。
プラットフォームの選択は、画一的なアプローチではなく、以下の点を考慮して行うべきです。
標的RNA送達システムの開発は、呼吸器医学に大きな進歩をもたらし、多様な肺疾患の分子メカニズムに対処するための新たな機会を提供しています。合成的および非合成的な送達プラットフォームの両方において、目覚ましい進歩が達成されていますが、臨床応用に向けては、依然としていくつかの重要な課題を克服する必要があります。
LNPs(リポペプチドナノ粒子)は、パターン認識受容体によって媒介される、用量依存的な細胞毒性と炎症反応を示します。特定のポリマー組成は、分子量や分解生成物に応じて細胞毒性を引き起こす可能性があります。組み込み能力を持つウイルスベクターは、挿入変異のリスクを伴います。
LNP(脂質ナノ粒子)の構成要素は、生体に対する固有の免疫応答経路を活性化する可能性があります。ペプチドベースのベクターは、非自己配列に対して応答を引き起こす可能性があります。ウイルスベクターは、強力な体液性および細胞性免疫にさらされ、既存の中和抗体の存在により、多くの患者において反復投与が著しく制限されることがあります。
エクソソームおよび生物学的ベシクルは、大規模生産、ロット間のばらつき、および異質な内容物の搭載において、大きな課題に直面しています。ベシクルの完全性を損なうことなく表面を修飾することは、臨床応用をさらに複雑にします。
LNPs(リポペプチドナノ粒子)は、生体液中での循環安定性が不十分であることが示されています。ペプチドベースのベクターは、急速な酵素分解を受け、循環半減期が短くなります。ポリマーシステムは、性能が様々であり、タンパク質キャリアは、多くの場合、生理的条件下で安定性に問題があります。
LNPs(リポペプチドナノ粒子)は、特定の組織への分布が制限されるという課題があります。ポリマーキャリアは、トランスフェクション効率が多様です。エクソソームは、合成システムと比較して、RNAの搭載効率が比較的低いという特徴があります。タンパク質キャリアは、エンドソームからの脱出能力が限定的です。
脂質化学、高分子科学、および生物学的キャリア工学における進歩の融合は、次世代の肺領域RNA治療薬が、複数の送達方法の補完的な利点を統合した、合理的に設計されたハイブリッドプラットフォームをますます活用するようになる可能性を示唆しています。
RNA送達技術の継続的な進化、および肺疾患のメカニズムに関する知識の拡大、そして患者個々の特性に関する理解の深化は、RNAベースの治療法の潜在的な治療効果を最大限に引き出し、最終的には呼吸器医学の分野全体を大きく変革する上で重要な役割を果たすでしょう。