薬物投与経路
薬物送達は、疾患の治療と予防において非常に重要な要素であり、薬物の安全性と有効性に直接影響を与えます。様々な送達システムが存在し、それぞれが異なる特徴を持っています。経路の選択は、以下の3つの重要な要素に依存します。
医薬品の性質
化学的性質(胃酸や消化酵素に対する感受性)、溶解性(脂溶性か水溶性か)、分子の大きさおよび構造、そして熱、光、または酸素に対する安定性。
薬理作用
作用部位(全身性のもの、例えば降圧剤、と局所性のもの、例えば点眼薬)、必要な放出速度(速効性 vs 徐放性)、そして標的細胞または臓器への到達性(一部の領域、例えば血液脳関門は、特別な設計が必要)。
患者の服薬遵守.
年齢や身体状態(乳幼児や高齢者は注射や大サイズの錠剤を服用できない場合がある)、受容性(一部の患者は注射よりも経口または吸入の方が好ましい)、および利便性(複雑な剤形は服薬アドヒアランスを低下させる可能性がある)。
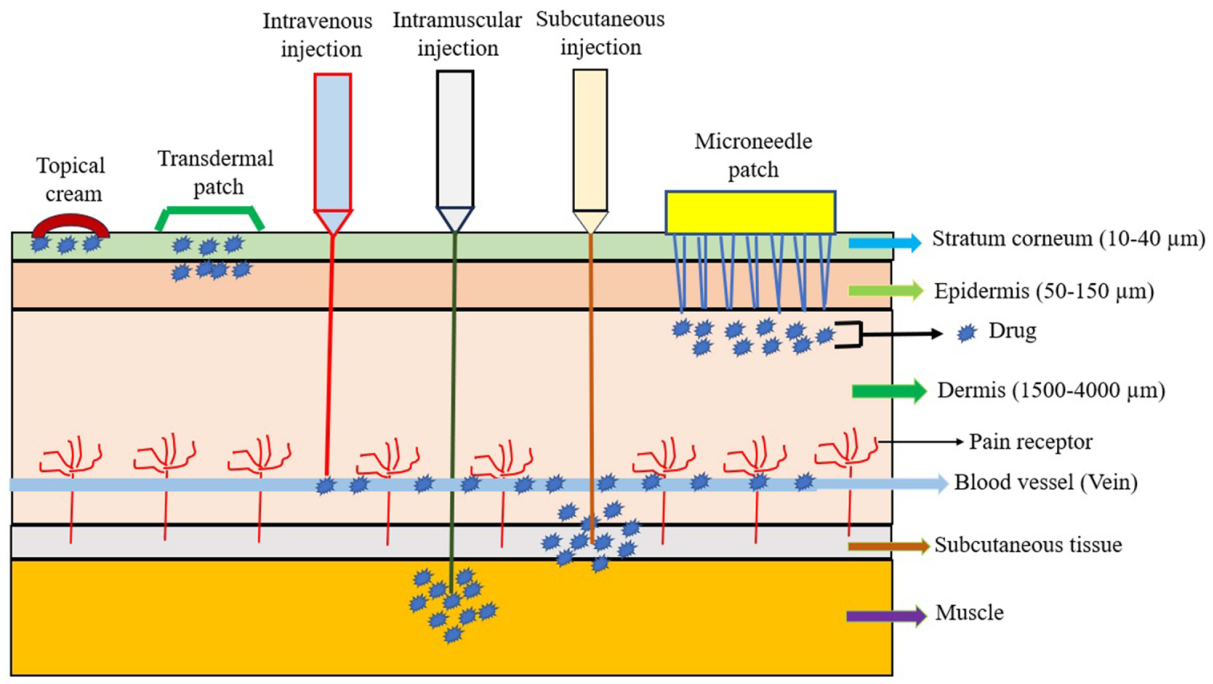
表1:薬物送達システムの比較
| Delivery | Topical Cream | Transdermal Patch | Oral | Intravenous | Intramuscular | Subcutaneous | Microneedle | Inhalation |
|---|---|---|---|---|---|---|---|---|
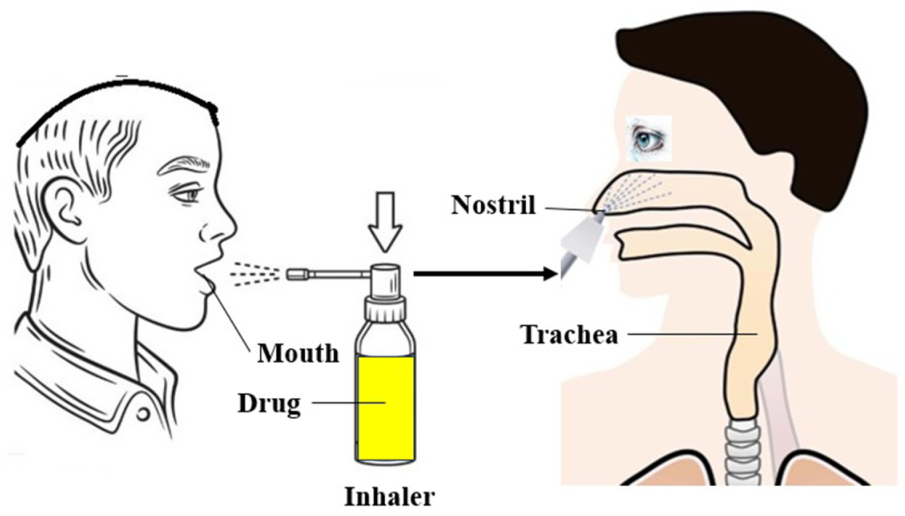
| Description | A cream to be smeared on the skin | An adhesive patch to be placed on the skin | Uptake of drugs by swallowing or drinking through mouth | An injection into a vein and directly into the bloodstream | An injection deep into the muscle to allow the bloodstream to absorb quickly | An injection given just on the subcutaneous tissues | Micro-size needles aligned on the surface of a small patch | Uptake of drugs by inhaler through mouths or noses |
| Mechanism | Drugs permeate through skin pores | Drugs permeate stratum corneum barrier and diffuse across the skin | Drugs enter the body through digestive tracts | Drugs placed directly in the vein | Drugs placed directly in the muscle | Drugs placed directly in the dermis | Drugs bypass stratum corneum, placed in epidermis or dermis | Drugs enter through respiratory tracts |
| Action | Local | Local | Systemic | Systemic | Systemic | Systemic | Systemic | Local or Systemic |
| Onset | Slow | Slow | Slow | Fast | Fast | Fast | Fast | Fast |
| Pain | No | No | No | Yes | Yes | Yes | No | No |
| Bioavailability | Poor | Insufficient | Insufficient | Sufficient | Sufficient | Sufficient | Sufficient | Sufficient |
| Self-admin | Yes | Yes | Yes | No | Possible | No | Yes | Yes |