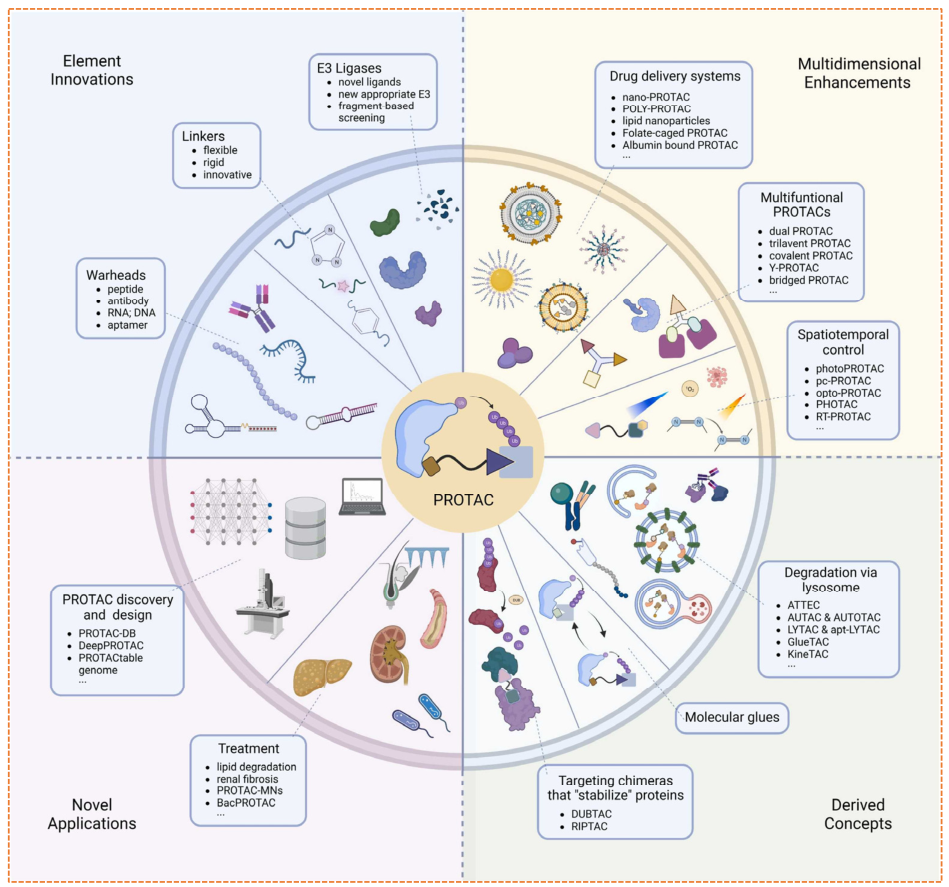
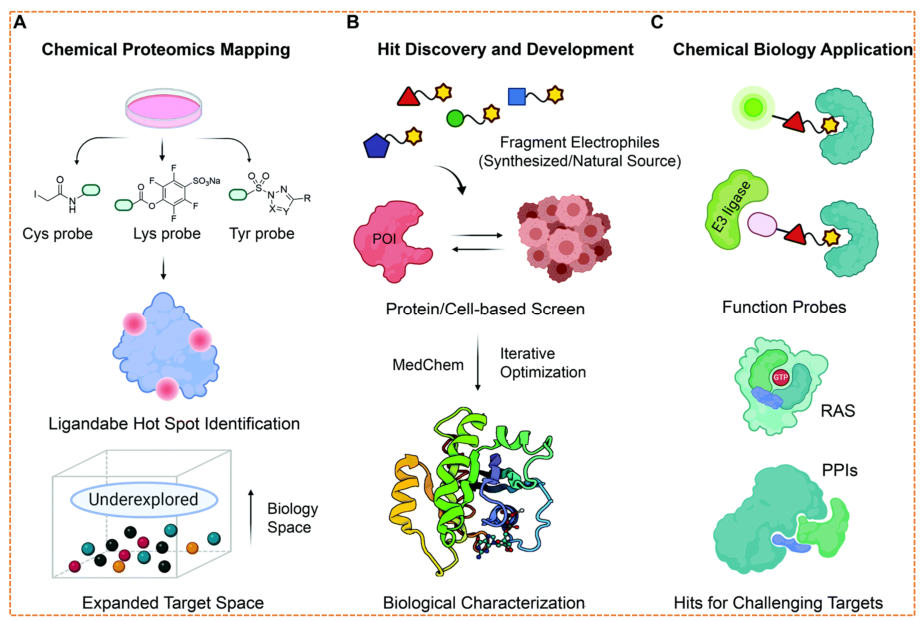
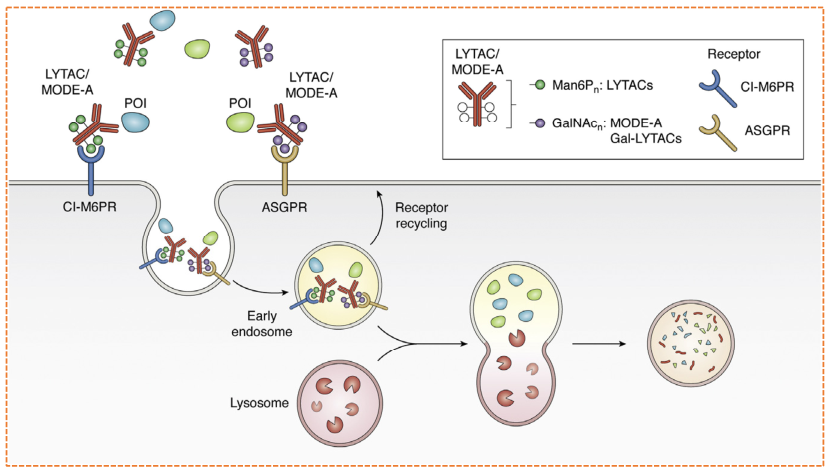
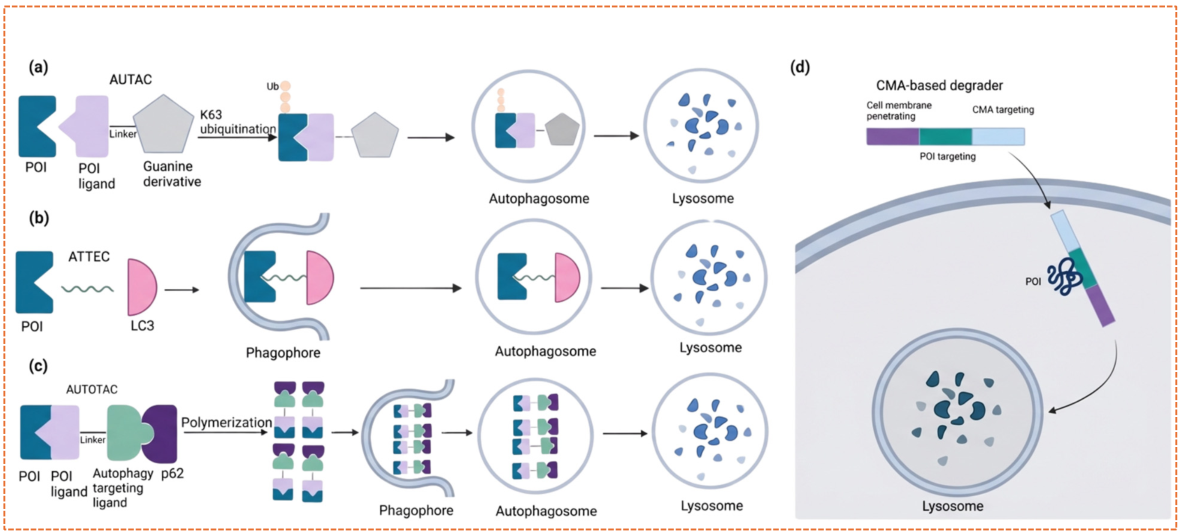
PROTAC設計の概要
作用機序
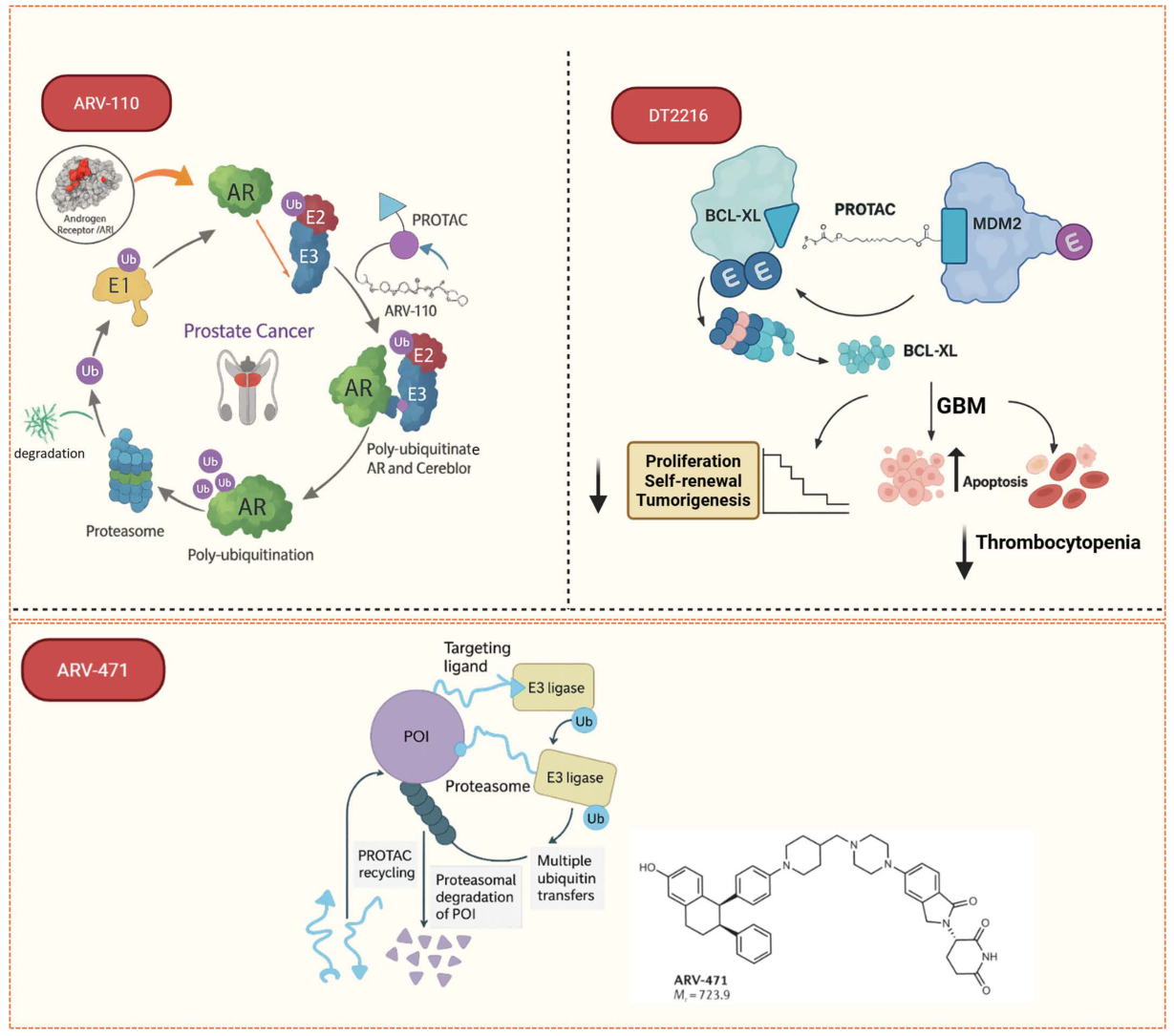
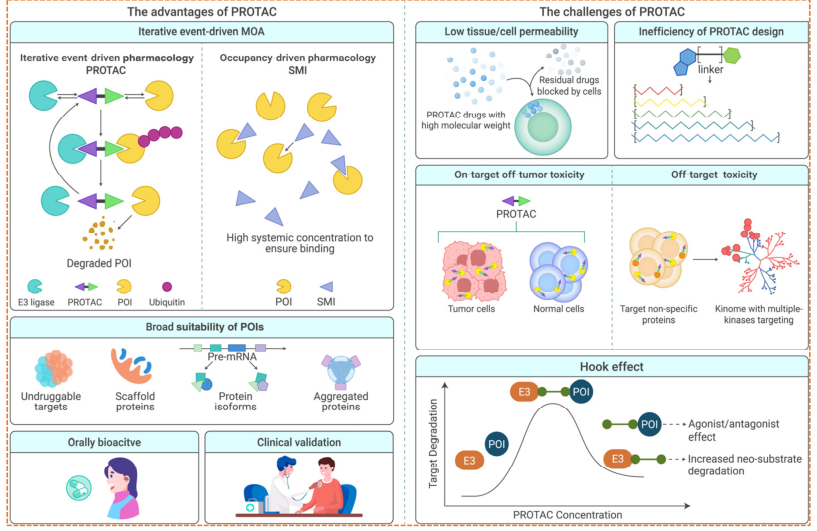
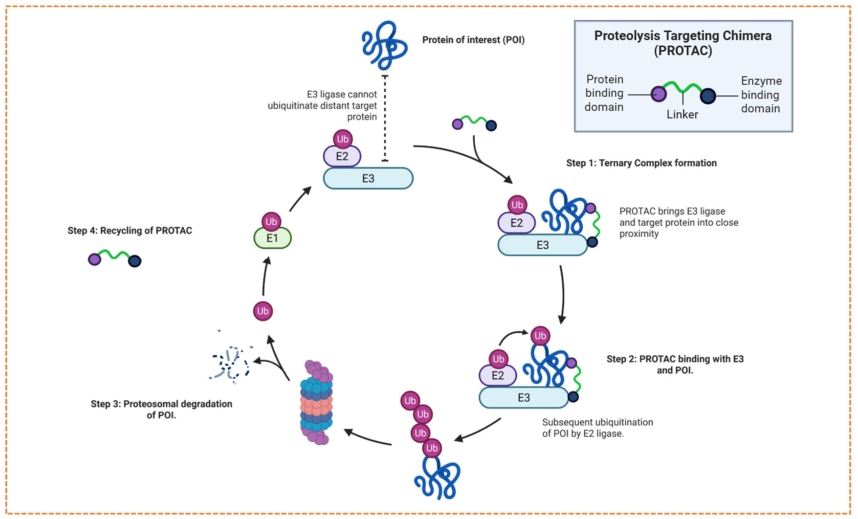
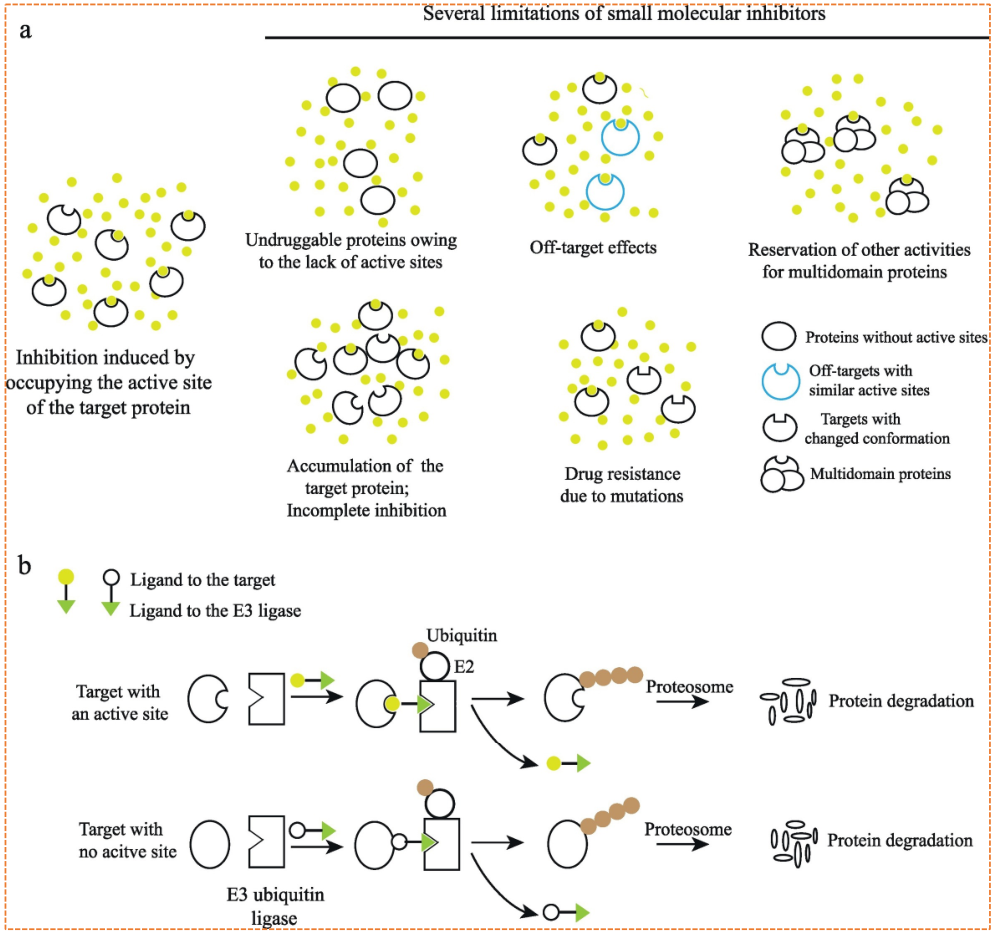
PROTACは、3つの必須の構造的構成要素で構成されています。それは、関心対象のタンパク質(POI)に結合するリガンド、E3ユビキチンリガーゼを募集するリガンド、そしてそれらを連結する化学リンカーです。PROTACがPOIとE3リガーゼを結合すると、ユビキチン伝達をトリガーする三元複合体が形成されます。多重ユビキチン化されたターゲット分子は、その後、26Sプロテアソームによって認識され、分解されます。重要なことに、PROTAC自体は分解後に再利用され、触媒的に追加のターゲット分子と反応することができます。
ユビキチン・プロテアソームシステム:細胞のリサイクル工場
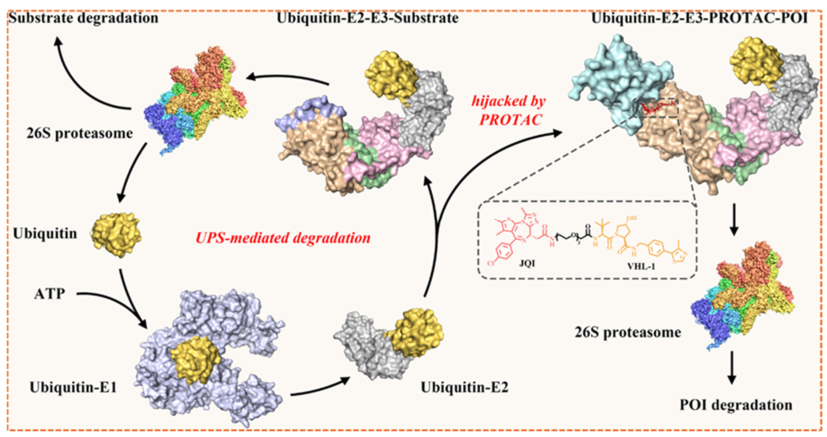
すべての細胞には、高度なリサイクルシステムが存在します。その仕組みは、以下の3つのステップで説明できます。
- E1(活性化):小さなタンパク質であるユビキチンが「活性化」され、スタンプをスタンプ機にセットするような状態になります。
- E2(転送):活性化されたユビキチンは、運び屋となる酵素に渡され、まるで郵便配達員にスタンプを渡すようなものです。
- E3(タグ付け):E3リガーゼは、どのタンパク質にユビキチン鎖を付加するかを決定する「判断者」です。PROTACsは、このステップを乗っ取り、E3リガーゼに特定の疾患関連タンパク質にタグを付加させます。
タンパク質がユビキチン分子の鎖でタグ付けされると、プロテアソーム(細胞のシュレッダー)によって認識され、アミノ酸の構成要素に分解されます。
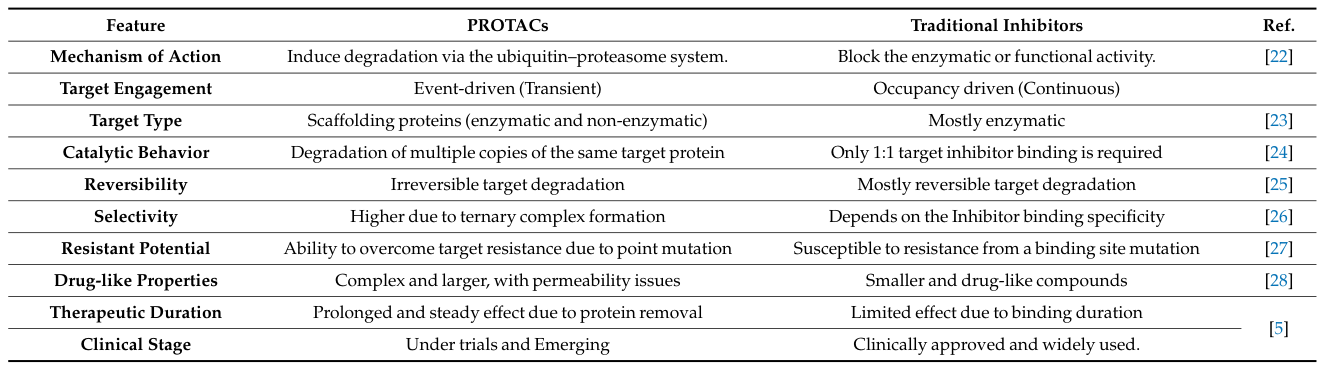
PROTACsと従来の阻害剤の比較
従来の低分子阻害剤には、いくつかの重要な限界があります。それらは、活性部位を持たないタンパク質を標的にできない、オフターゲット効果がある、不完全な阻害しか達成できない、そして、耐性変異の影響を受けやすい、といった問題があります。PROTACsは、これらの問題を克服するために、タンパク質の機能を単純に阻害するのではなく、タンパク質全体を分解することで作用します。分解は、標的タンパク質の酵素的機能と構造的機能の両方を排除するため、PROTACsは、阻害剤では対応できない標的や耐性メカニズムに対処することができます。
E3リガーゼがPROTAC設計において果たす役割
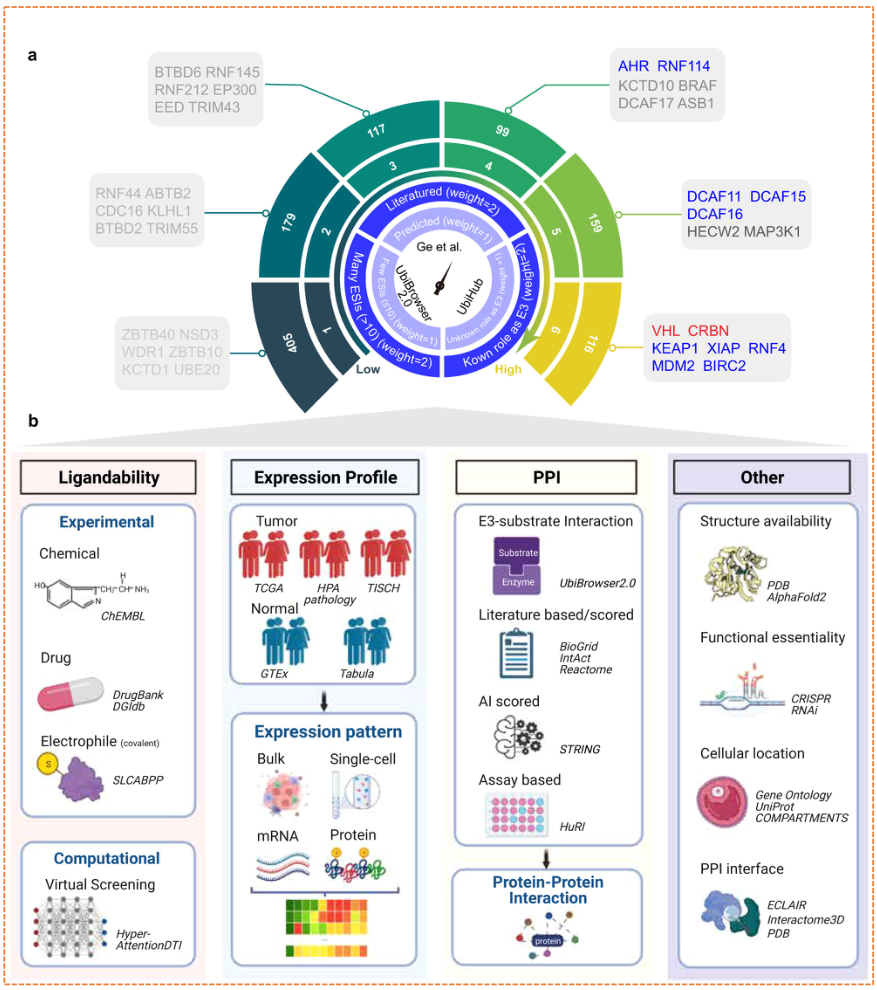
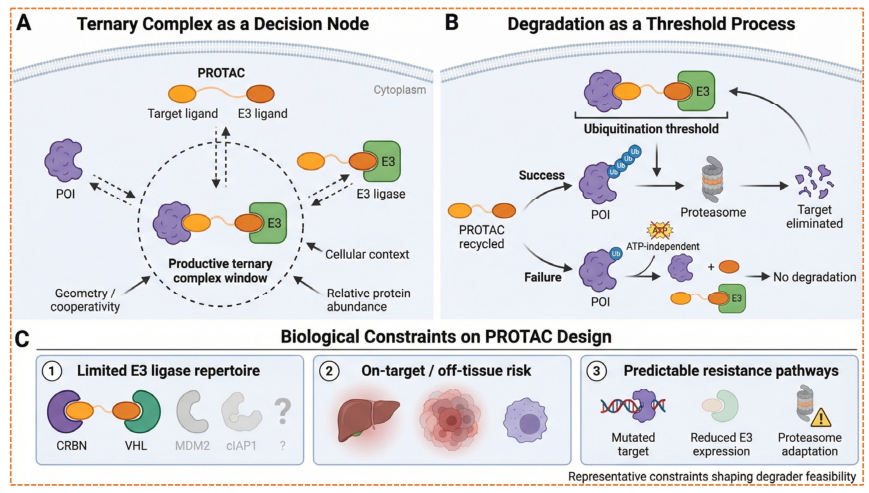
人間のゲノムは約600種類のE3ユビキチンリガーゼをコードしていますが、現在のPROTAC技術は主に2種類のみを利用しています。それはCRBN (cereblon)とVHL (Von Hippel-Lindau)です。これら2つが現在開発中のPROTACのほとんどを占めています。E3リガーゼのバリエーションを増やすことは、組織特異性を広げ、オフターゲット効果を低減し、リガーゼのダウンレギュレーションによって生じる薬剤抵抗性を克服するために不可欠です。新たに発見されたE3リガーゼのターゲットとしては、KEAP1、MDM2、XIAP、RNF4、およびBIRC2などが挙げられ、これらは化学プロテオミクスや計算アプローチによって明らかにされました。
なぜ600種類のうちわずか2種類なのか?
ヒトゲノムは、約600種類のE3リガーゼをコードしていますが、PROTACの研究者は、ほとんどの場合、以下の2種類のみを使用します:CRBNとVHL。その理由は、これら2種類が、それぞれ特徴よく研究された低分子リガンド(CRBNの場合は、タリドミド誘導体、VHLの場合は、特定のペプチド模倣体)を持っているからです。これは、600人の鍵屋がいる都市に住んでいても、電話番号を知っているのが2人だけのようなものです。現在、他のE3リガーゼの「電話番号」を発見し、組織特異的で耐性を持たないPROTACを実現するための研究が進められています。
PROTAC設計における最近の革新
PROTAC分野では、リンカー化学、空間的/時間的制御、および送達システムにおいて、急速な技術革新が見られています。
- Photo-PROTACs: 光によって活性化されるPROTACであり、タンパク質の分解を時間空間的に制御し、健康な組織におけるオフターゲット効果を低減します。
- Click-PROTACs: 細胞内でのPROTAC構成要素の、生体直交クリック化学を利用した組み立て。これにより、腫瘍選択的な活性化が可能になります。
- フォレート封入型PROTACs: 腫瘍を標的とするPROTACであり、フォレート受容体を発現している癌細胞でのみ活性化され、治療効果を高める。
- 共有結合PROTACs: 標的分子またはE3リガーゼのいずれかへの不可逆的な結合により、有効性を高め、持続的な分解を促進します。