
レビュー論文 — ACS Pharmacology & Translational Science, 2026
エピジェネティクスの未来
新技術と臨床応用

レビュー論文 — ACS Pharmacology & Translational Science, 2026
新技術と臨床応用
エピジェネティクスは、DNA配列自体への変化を伴わずに起こる、遺伝可能な遺伝子発現の変化を研究する分野です。エピジェネティック機構は、遺伝コードそのものを変化させるのではなく、DNA、ヒストンタンパク質、およびRNA分子に対する化学修飾を通じて、遺伝子をオンまたはオフにする、DNAの上にある制御層として機能します。
本包括的なレビューでは、CAS Content Collection に収録された 120,000件以上のエピジェネティクス関連文献 (2000–2024) のデータを用いて、この分野の目覚ましい発展を明らかにします。主要な 4 つのエピジェネティックメカニズム — DNA メチル化, ヒストン修飾, ノンコーディング RNA (ncRNA), および クロマチンリモデリング — がそれぞれ詳細に解説され、健康と疾患におけるそれぞれの役割についても議論されます。
臨床的な影響は劇的であり、13種類のFDA(米国食品医薬品局)承認済みのエピジェネティクス医薬品が現在市場に流通しており、主に血液のがんを標的としています。さらに、37件以上の臨床試験が進行中で、代謝、神経、および炎症性疾患への応用が広がっています。2023年の世界のエピジェネティクス市場の規模は18億4000万ドルと評価されており、2033年には67億7000万ドルに達すると予測されています。
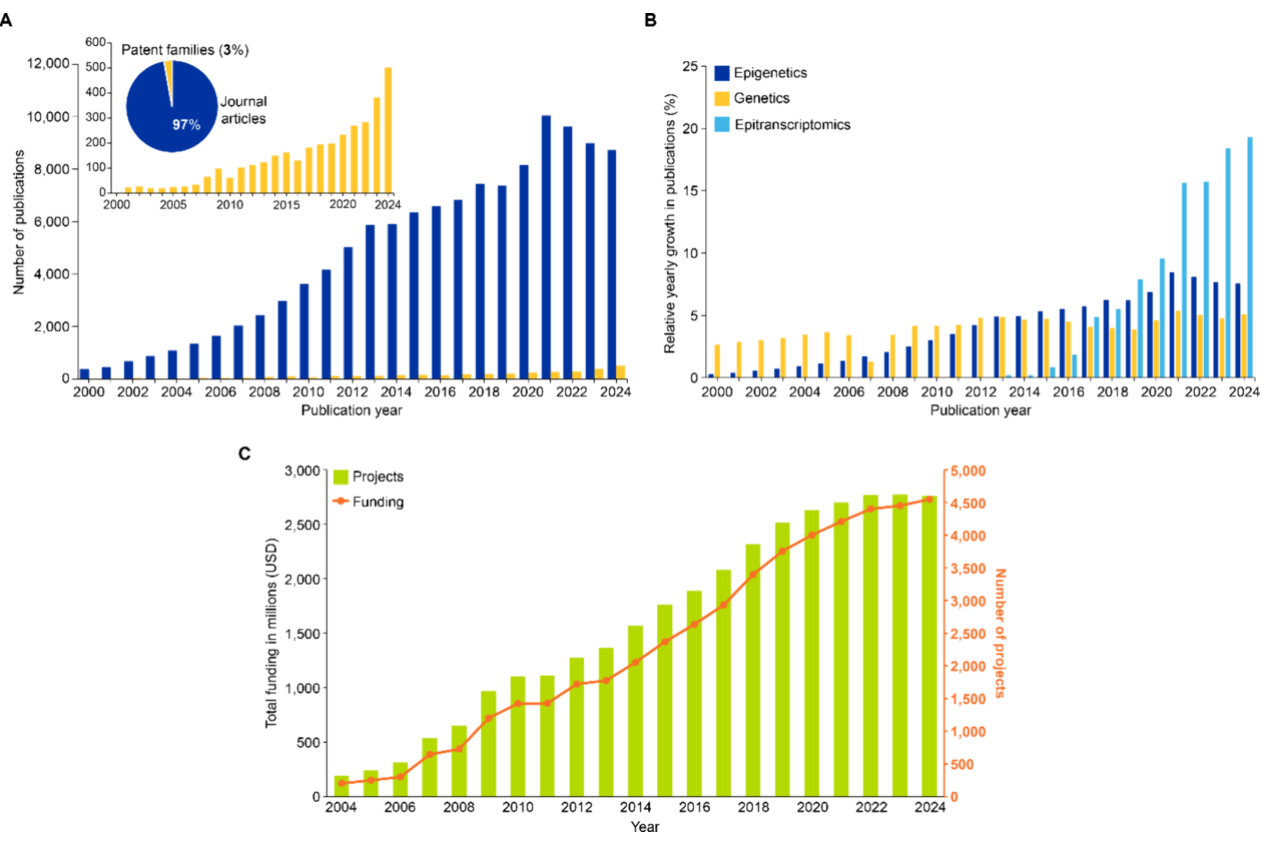
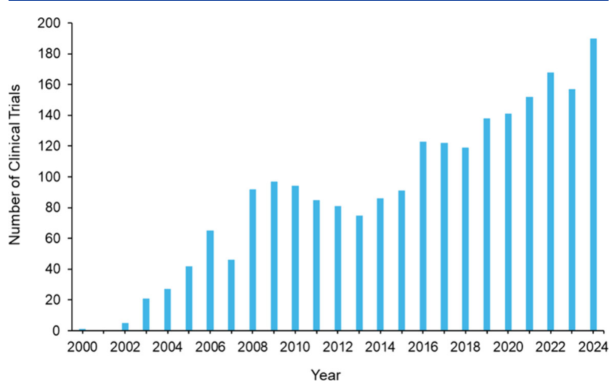
CAS Content Collectionには、2000年から2024年までのエピジェネティクス関連の出版物が12万件以上含まれており、研究成果の著しい加速を示しています。出版件数は、2000年代初頭の年間数百件から、現在では年間12,000件以上に増加しています。特許および資金調達も同様の傾向を示しており、この分野の商業的な重要性を強調しています。
エピジェネティックな制御は、DNA配列を変えることなく遺伝子発現を制御する、主に4つの化学修飾によって行われます。各メカニズムは、DNAそのものを修飾することから、DNAが巻き込まれるタンパク質の構造を再構築することまで、異なるレベルで作用します。
最も研究されているエピジェネティックなマーカー。メチル基(–CH3)は、CpG部位のシトシン塩基に付加され、通常、遺伝子発現を抑制します。DNMT酵素によって触媒されます。DNMT1は、細胞分裂中にパターンを維持し、DNMT3a/3bは新しいパターンを確立します。X染色体不活性化、ゲノムインプリンティング、および胚発生に不可欠です。異常なメチル化(例えば、腫瘍抑制遺伝子の抑制など)は、がんの重要な特徴です。
CpGサイトとは、DNA上のシトシン(C)がグアニン(G)に続く場所のことです。“p”は、これらを繋ぐリン酸ジエステル結合を指します。これらのサイトは、スイッチのような役割を果たします。メチル基がこれらのサイトに付加されると、近くにある遺伝子がオフになります。これは、ペンにキャップをかけるイメージです。ペン(遺伝子)はまだ存在しますが、書くこと(発現)ができません。
DNMT(DNAメチルトランスフェラーゼ)は、これらのメチルキャップを付加する酵素です。DNMT1は、細胞分裂時に既存のメチル化パターンをコピーする「メンテナンス担当」、一方、DNMT3aとDNMT3bは、胚発生中に新しいメチル化マーカーを作成する「設置チーム」です。
翻訳後修飾(アセチル化、メチル化、リン酸化、ユビキチン化)は、ヒストンタンパク質に作用し、DNAがどの程度に巻き込まれるかに影響を与えます。アセチル化は染色体を緩めます(遺伝子の活性化)、一方、脱アセチル化は染色体を締め付けます(遺伝子の抑制)。これは、HAT(書き込み酵素)とHDAC(消去酵素)によって制御されます。異常なヒストン修飾は、遺伝子発現を阻害し、癌、神経変性疾患、およびその他の疾患に寄与します。
HATs と HDACs: DNA を糸が糸巻き(ヒストン)に巻き付いているものだと考えてください。HATs(ヒストンアセチル転移酵素)は、アセチル基を付加することで糸を緩め、遺伝子が読み取り可能になるようにします。一方、HDACs(ヒストン脱アセチル化酵素)は、その逆の働きをします。つまり、巻きを締め、遺伝子を細胞の読み取り機構から隠します。多くの抗がん剤は、HDACs を阻害することで、腫瘍抑制遺伝子を再活性化する作用があります。
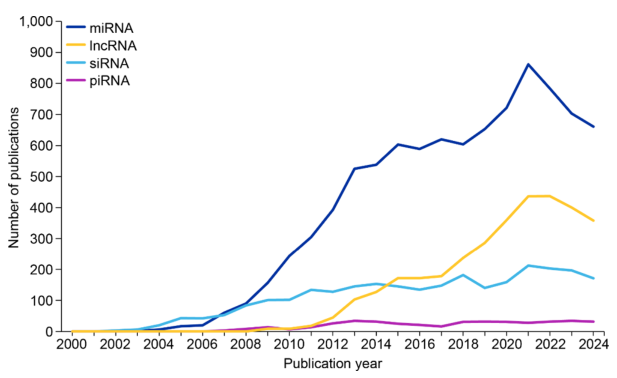
タンパク質をコードしないが、遺伝子発現を制御する制御性RNA分子。 miRNAs (最も研究されている、ピークは2021年) は、標的となるmRNAを分解します。lncRNAs (急速に成長中) は、クロマチン修飾複合体を特定のゲノム領域に誘導します。piRNAs は、生殖細胞におけるトランスポゾン要素を抑制します。全体として、ncRNAは、遺伝子制御の洗練された翻訳後段階を形成します。
ATP依存性タンパク質複合体(SWI/SNF、ISWI、CHD、INO80)は、ヌクレオソームの物理的な構造を再構成し、遺伝子制御領域を露出させたり隠したりする。SWI/SNFの変異は、ヒトのがんの約20%で見られる。この4つのメカニズムの中で最も研究が進んでいないが、発生や疾患において非常に重要であることが認識されつつある。
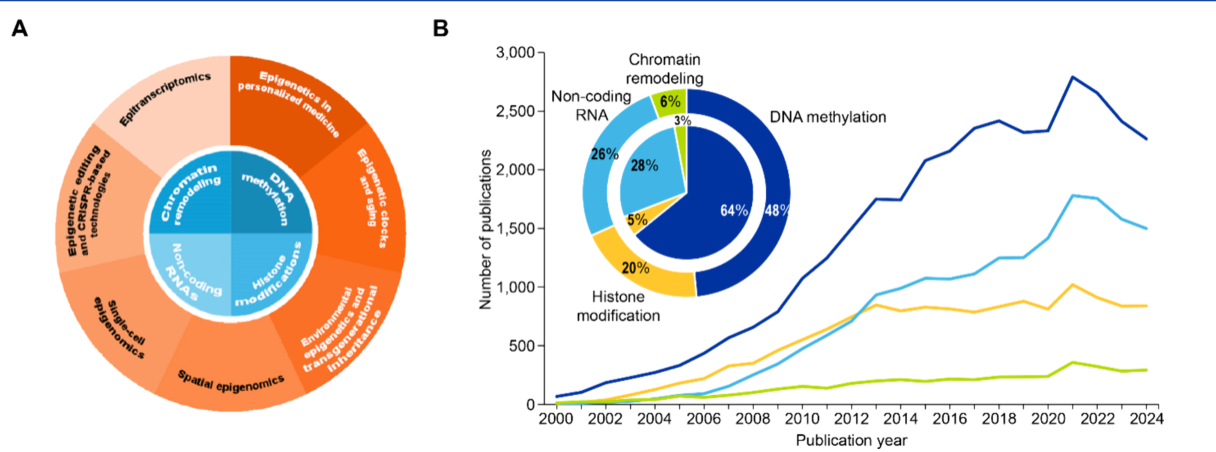
従来の4つの主要なメカニズムに加えて、6つの新しい研究分野が、エピジェネティック制御に対する私たちの理解を深め、新たな治療法の可能性を開拓しています。
RNAに対する170種類以上の異なる化学修飾の研究. 最も豊富に存在するものは、N6-メチルアデノシン(m6A)であり、これは「ライター」(METTL3/14)、「イレーザー」(FTO, ALKBH5)、および「リーダー」(YTHDFタンパク質)によって制御されます。 これらの修飾は、mRNAの安定性、スプライシング、および翻訳に影響を与え、がん、肥満、および神経疾患との関連が示唆されています。
エピトランスクリプトミクスは、DNAエピジェネティクスと同じ考え方を、RNA分子に適用したものです。DNAがメチル化によって修飾されるように、RNAも化学的修飾を受け、その挙動が変化することがあります。
この分野では、覚えやすいフレームワークが用いられています。
最も研究されているRNAの修飾は、m6A (N6-メチルアデノシン)であり、mRNA分子の生存期間、その加工、およびタンパク質の合成効率に影響を与えます。このシステムにおける異常は、癌、肥満、および神経疾患との関連が報告されています。
非活性化されたCas9 (dCas9) に、エピジェネティック効果ドメインを融合させることで、DNA配列を変更することなく、特定のゲノム領域におけるエピジェネティックな修飾を改変することができます。CRISPRiは遺伝子を抑制し、CRISPRaは遺伝子を活性化します。これは、恒久的な遺伝子編集に対する、潜在的に可逆的な代替手段であり、研究成果は急速に増加しており(2020年から2024年にかけて3倍に増加)。
従来のCRISPRによる遺伝子編集は、遺伝子を不活性化するためにDNAを恒久的に切断します。一方、エピジェネティックCRISPRは異なります。不活性化されたCas9(dCas9と呼ばれる)を使用し、特定の遺伝子を特定できますが、切断はしません。代わりに、エピジェネティックツールを搭載しており、クロマチンを修飾することで、遺伝子を抑制(CRISPRi = CRISPR干渉)または活性化(CRISPRa = CRISPR活性化)します。DNAが切断されないため、変化は潜在的に可逆的であり、これは、恒久的なゲノムの変化がリスクを伴う治療用途において、大きな利点となります。
シングルセル技術(scATAC-seq, scBS-seq)は、組織内の個々の細胞間で存在するエピジェネティックな多様性を明らかにします。空間エピジェノミクスは、最新の研究分野であり、組織のコンテキストにおけるエピジェネティックなマーカーをマッピングします。これらは組み合わせて、腫瘍の多様性、発生経路、細胞タイプ特異的な制御を理解することを可能にします。
最も活発な研究分野(年間300~400件の論文)。環境要因(食生活、ストレス、毒素、ライフスタイルなど)は、DNAの配列変化を伴わずに、世代を超えて持続する遺伝可能なエピジェネティックな変化を引き起こす可能性があります。これは公衆衛生政策に大きな影響を与えます。親が汚染や栄養不足にさらされることは、子や孫に世代を超えたエピジェネティックな遺伝を通じて影響を与える可能性があります。
世代を超えたエピジェネティックな遺伝は、長年信じられてきた生物学的な仮説に挑戦します。それは、後天的に獲得された特性は子孫に受け継がれない、という考え方です。DNA配列は変化しませんが、環境要因によって引き起こされるエピジェネティックな変化は、卵子や精子を通して将来の世代に伝えられる可能性があります。
よく知られた例として、オランダの飢饉(1944~45年)では、妊娠中に飢餓を経験した母親の子供たちは、数十年後に肥満や心血管疾患の発生率が高いことが示されました。そして、一部の効果は、直接的な曝露を受けていない孫にも見られました。これは、環境政策に大きな影響を与えます。今日の工業的な汚染や食習慣が、エピジェネティックなメカニズムを通じて、将来の世代の健康に影響を与える可能性があるからです。
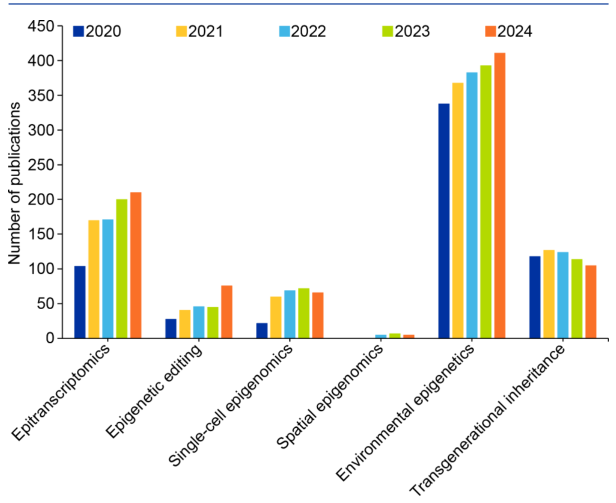
エピジェネティックな異常は、広範なヒトの疾患の基盤となっています。疾患に関連するエピジェネティクスに関する出版物全体の中で、最も多いのが癌で、47%を占め、次いで老化(9%)、感染症、神経疾患、代謝性疾患、自己免疫疾患が挙げられます。この分野は、現在、腫瘍学の枠を超えて積極的に発展しています。
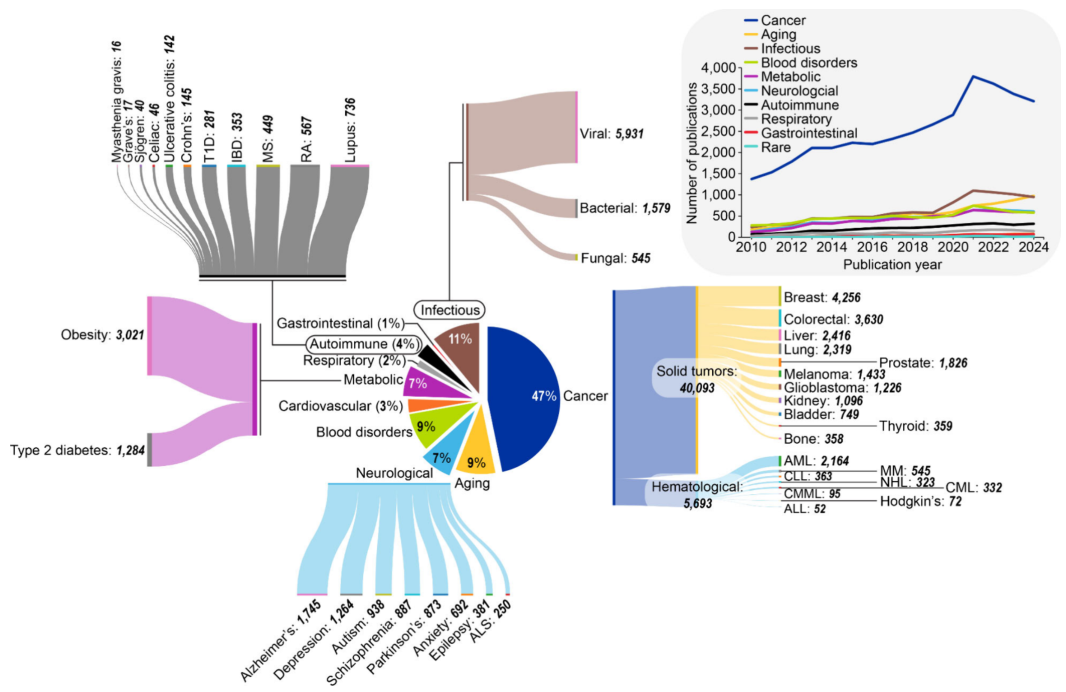
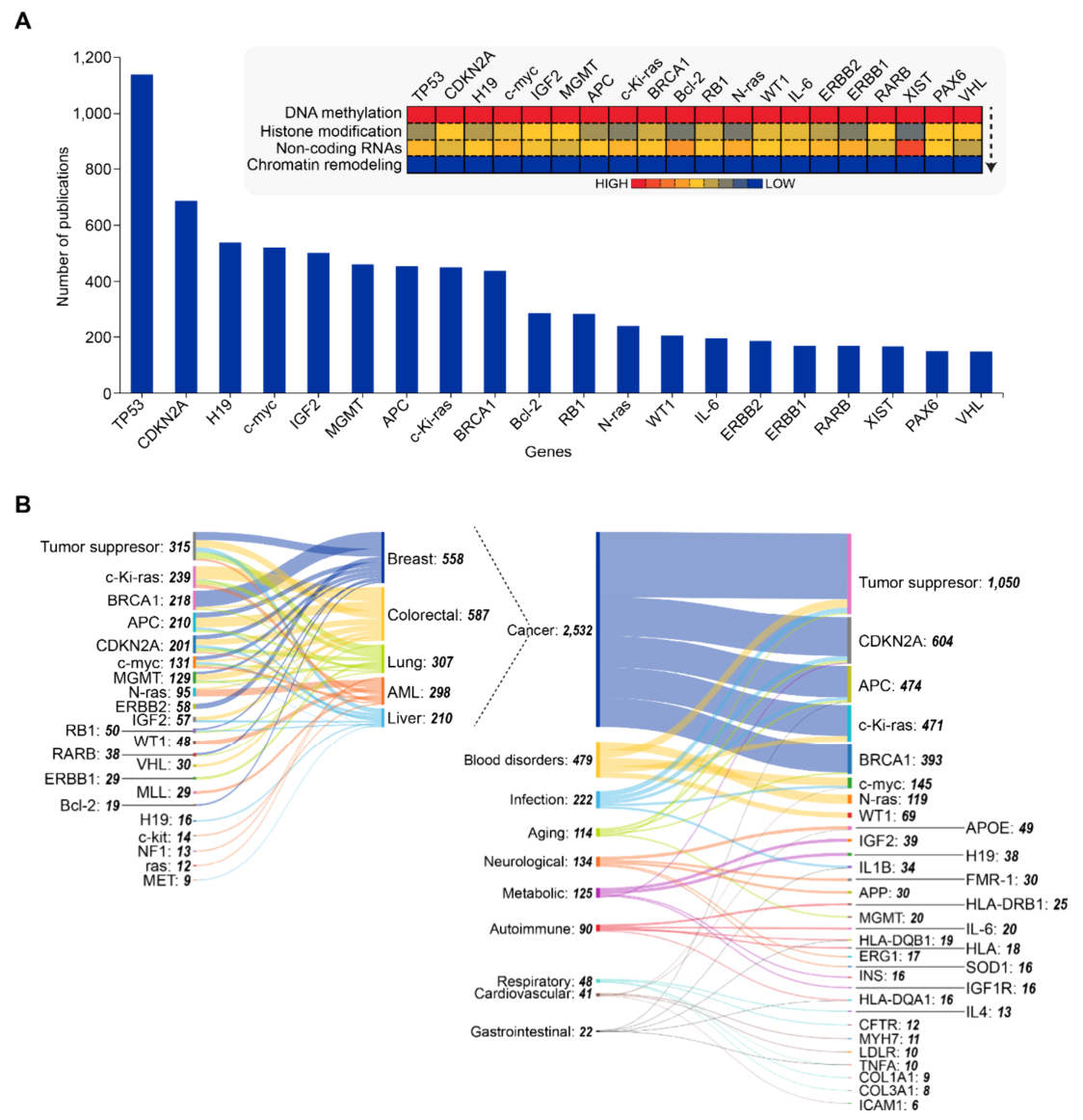
エピジェネティック疾患研究の最も大きな分野は47%を占めます。異常なDNAメチル化、ヒストン修飾、およびncRNAの機能不全が腫瘍の発生を促進します。TP53は最も研究されている遺伝子であり(1,200件以上の論文)、次いでCDKN2A、H19、c-myc、およびIGF2が挙げられます。プロモーターの過剰メチル化による腫瘍抑制遺伝子の沈黙、および低メチル化による癌遺伝子の活性化が主要なメカニズムです。乳がんおよび大腸癌は、最も集中的に研究されている腫瘍型です。
エピジェネティックなクロックは、DNAメチル化パターンから生物学的な年齢を予測する計算モデルです。主なものとしては、Horvathのクロック(2013年、353のCpGサイト、多組織)、Hannumのクロック(血液由来)、GrimAge(死亡予測)、そしてDunedinPACE(老化の速度)があります。これらのツールは、寿命、加齢に関連する疾患、そしてカロリー制限や運動といった介入が生物学的な老化に及ぼす影響に関する研究を可能にします。
あなたの暦年齢(誕生からの年数)と、生物学的年齢(あなたの体が実際に「どれくらいの年齢」に見えるか)は、大きく異なることがあります。エピジェネティック・クロックは、特定のゲノム領域におけるDNAメチル化パターンを分析することで、生物学的年齢を測定します。
例えば、Horvathのクロックは、353の特定のCpG部位におけるメチル化を調べ、数学モデルを用いて生物学的年齢を予測します。50歳で、60歳の人と同じメチル化パターンを持つ人は、生物学的な老化が加速している状態であり、これは潜在的に、より高い疾患リスクを示唆する可能性があります。逆に、一部の生活習慣の改善(運動、カロリー制限など)は、エピジェネティック・クロックを遅らせるように見えます。
GrimAgeは、さらに進んで、死亡リスクを予測します。一方、DunedinPACEは、老化の速度(現在、どれくらいの速さで老化しているか)を測定し、臨床試験におけるアンチエイジング介入の効果を評価するのに役立ちます。
異常なエピジェネティックな変化は、アルツハイマー病、パーキンソン病、およびハンチントン病に寄与する。DNAメチル化およびヒストンアセチル化のパターンが変化することで、神経細胞の機能に重要な遺伝子に影響を与える。HDAC阻害薬は、神経変性疾患における記憶とシナプス可塑性を回復させるための前臨床モデルにおいて有望な結果を示している。
2型糖尿病は、インスリンシグナル伝達に関わる遺伝子(例:*INS*, *IGF1R*)におけるDNAメチル化の変化と関連しています。肥満は、*FTO*遺伝子のメチル化を介してエピゲノムを変化させます。自己免疫疾患(リウマチ、ループス、多発性硬化症など)は、免疫細胞の分化と機能におけるエピジェネティックな異常を伴い、その共通の特徴として、広範囲なDNAの低メチル化が挙げられます。
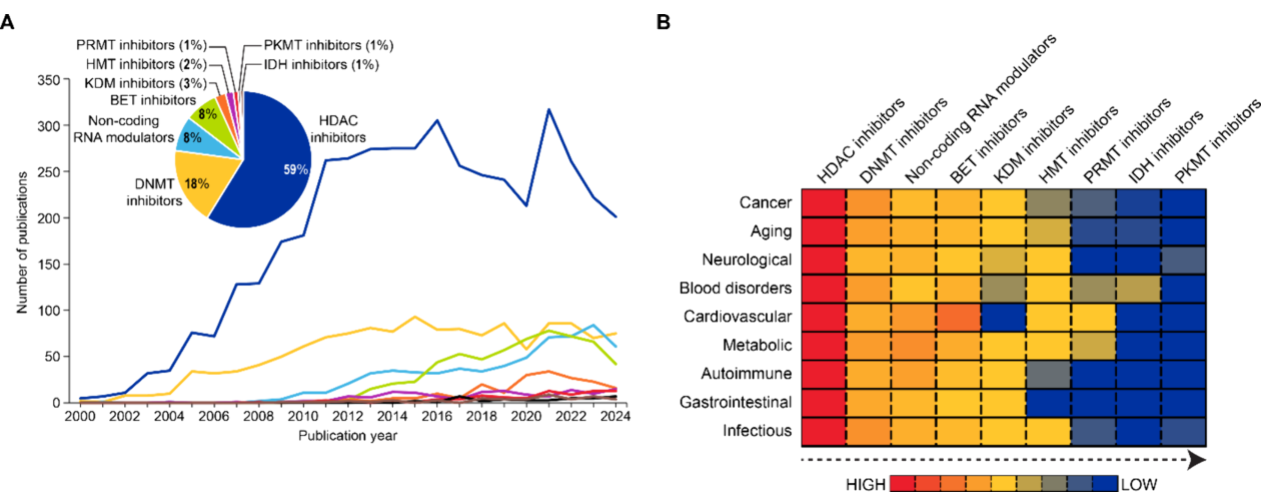
エピジェネティック薬(epi-drugs)は、異常なエピジェネティック修飾を逆転させることで、正常な遺伝子発現を回復する作用を持ちます。治療の分野は、HDAC阻害剤(論文の59%)が主流であり、次いでDNMT阻害剤(13%)が続きます。合計で13種類の薬剤がFDAの承認を受けており、主に血液悪性腫瘍に使用されていますが、現在では非癌の適応にも広がっています。
従来の抗がん剤は、遺伝子変異や急速に分裂する細胞を標的とします。一方、エピ遺伝学的薬剤(Epi-drugs)は、根本的に異なるアプローチをとります。具体的には、遺伝子が異常な働きをする原因となっている化学修飾を逆転させます。例えば、HDAC阻害薬は、がん細胞を直接殺すのではなく、クロマチンを再構成し、沈黙している腫瘍抑制遺伝子が再び機能するようにします。これは、がん細胞が正常な働きをするように「思い出させる」ことになります。このため、エピ遺伝学的薬剤は、しばしば「再プログラム」療法と呼ばれます。
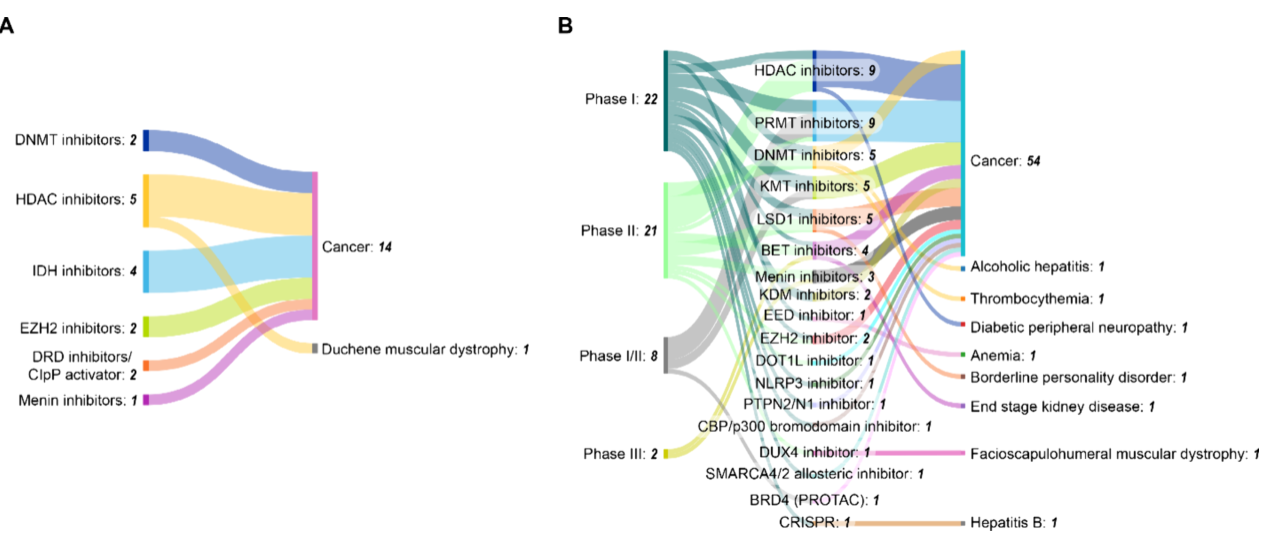
エピジェネティック医薬品の臨床試験の状況は劇的に拡大しており、25年間にClinicalTrials.govに登録された試験は、なんと2,200件にのぼります。第II相試験が最も多くを占めており(57%)、これは多くの併用療法戦略が探索的な性質を持っていることを反映しています。注目すべきは、62%の試験がすでに承認されている薬剤を対象としている点であり、これは広範な適応拡大の取り組みを示唆しています。
| Phase | % |
|---|---|
| Early Phase I | 1% |
| Phase I | 32% |
| Phase II | 57% |
| Phase III | 9% |
| Phase IV | 1% |
| Status | % |
|---|---|
| Not yet recruiting | 4% |
| Recruiting | 17% |
| Active | 7% |
| Completed | 36% |
| Withdrawn | 36% |
特定の遺伝子座における修飾を行うために、エピジェネティック効果因子と融合したdCas9を使用します。これは、恒久的なDNAの変化を伴わずに、標的を絞った、潜在的に可逆的な治療を提供します。鎌状赤血球症を含む疾患に対する初期段階の臨床開発が進められています。
プロテオリアーゼを標的とするキメラは、ユビキチン-プロテアソームシステムを動員し、BRD4やEZH2などのエピジェネティック制御因子を選択的に分解します。これは、従来の酵素阻害という手法の代替となり得るものです。
PROTACs(プロテオリアシス・ターゲティング・キメラ)は、次世代のアプローチです。従来の酵素阻害剤とは異なり、PROTACsは分子シャペロンとして機能します。片端が標的タンパク質(例:BRD4)に結合し、もう片端が細胞が持つ自然のタンパク質分解システム(ユビキチン・プロテアソーム)を誘導します。これにより、標的タンパク質は分解され、完全に除去されます。この「阻害するのではなく、分解する」という戦略は、従来の阻害剤では発生する薬剤耐性を克服することができます。
エピジェネティック制御RNA(例:HOTAIRやMALAT1などのlncRNA)を標的とする、分解を促す短い合成核酸。発がん性のあるノンコーディング転写物を精密に抑制することを可能にします。
がん細胞において発現が抑制されている、腫瘍抑制効果を持つmiRNAの機能を回復させるように設計された合成分子。腫瘍細胞における正常な翻訳後遺伝子制御を再確立することを目的とする。
Pelabresib (CPI-0610) — 骨格制御タンパク質阻害薬であり、骨髄線維症のIII相臨床試験(MANIFEST-2試験)で使用されています。2019年にFDAの優先審査指定(Fast Track Designation)を受けました。 Ziftomenib (KO-539) — メニン-KMT2A阻害薬であり、2024年にFDAのブレークスルー・セラピー指定(Breakthrough Therapy designation)を受け、再発/難治性のNPM1変異型急性骨髄性白血病(AML)に使用されます。
Apabetalone (RVX-208) — BD2ドメインを標的とする選択的BET阻害剤であり、末期腎疾患に対する第I/II相試験を実施中。以前に、主要な心血管イベントに対するブレークスルーセラピー指定を受けていた。 Larsucosterol (DUR-928) — 最初のクラスのエピジェネティック調節薬であり、アルコール性肝炎に対する第II相試験を実施中。2024年にブレークスルーセラピー指定を受けた。
Vafidemstat (ORY-2001) — 境界性パーソナリティ障害に対するII相試験における選択的LSD1阻害薬であり、エピジェネティック治療の新しい神経精神医学的応用です。Givinostat — EUでデュシェンヌ型筋ジストロフィーの治療薬として承認されているHDAC阻害薬であり、エピジェネティック薬が腫瘍学の枠を超えて広がっていることを示しています。
エピジェネティックバイオマーカーは、エピジェネティックな修飾から得られる分子的な特徴であり、疾患の診断、予後予測、および治療効果のモニタリングに利用できます。 遺伝子変異とは異なり、エピジェネティックな変化は多くの場合可逆的であり、組織特異的であるため、非侵襲的な液体生検アプローチにおいて特に有用です。
最も臨床的に進歩したクラス。 SEPT9メチル化は、血液検査(Epi proColon)による非侵襲的な大腸がんスクリーニングを可能にします。 MGMTメチル化は、グリオブラストにおけるテモゾロミドへの反応を予測し、治療方針の決定に役立ちます。BRCA1およびp16プロモーターの過剰メチル化は、がんの重要な特徴です。
SEPT9メチル化検査(Epi proColonとして販売)は、画期的な進歩を意味します。大腸がんのスクリーニングに内視鏡検査が必要となる代わりに、簡単な血液検査によって、腫瘍細胞から血液中に放出される異常なDNAメチル化パターンを検出できます。同様に、グリオブラスト腫患者におけるMGMTメチル化検査は、医師がテモゾロマイドを処方するかどうかを判断するのに役立ちます。MGMTプロモーターがメチル化されている患者は、この化学療法薬に対して有意に良好な反応を示します。これらの例は、エピジェネティックバイオマーカーが精密医療を可能にしていることを示しています。つまり、患者の分子プロファイルに基づいて、特定の治療法を患者に適合させるということです。
特定のヒストン修飾は、疾患の指標として機能します。H3K27me3 のレベルは、がんの予後と相関します。H3K4me1 は、活性化エンハンサーに存在し、細胞タイプ特有の制御状態を特定することができます。グローバルなヒストンアセチル化レベルは、複数のがんでの予後予測に有用です。
循環するmiRNAは、非侵襲的な診断の可能性を提供します。miR-21とmiR-155は、複数の癌の種類において異常な発現を示します。HOTAIRやMALAT1などのlncRNAは、診断および予後価値があります。細胞外小胞にパッケージされたncRNAは、安定した血液由来のバイオマーカーとして注目されています。
ATAC-seqによるクロマチンアクセシビリティプロファイルは、腫瘍の分類とサブタイプ分類を可能にします。クロマチンアクセシビリティのパターンは、がんのサブタイプを区別し、治療反応を予測することができます。まだ発展途上ですが、急速な技術的進歩により、臨床応用が現実のものになりつつあります。
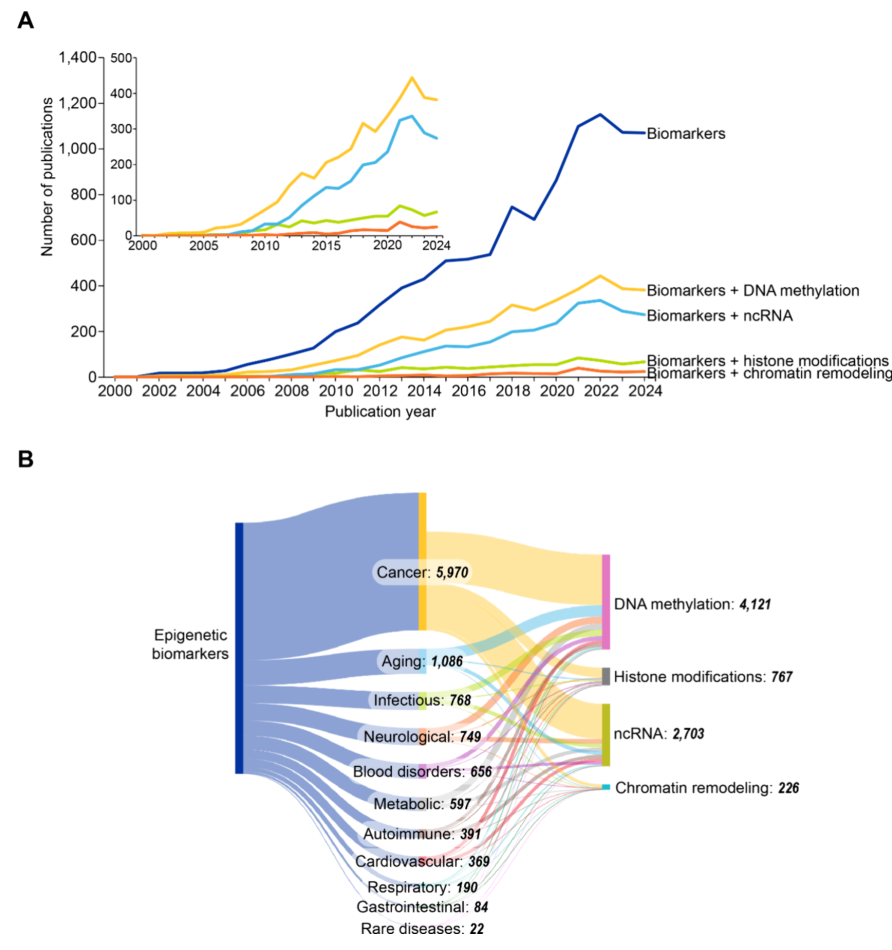
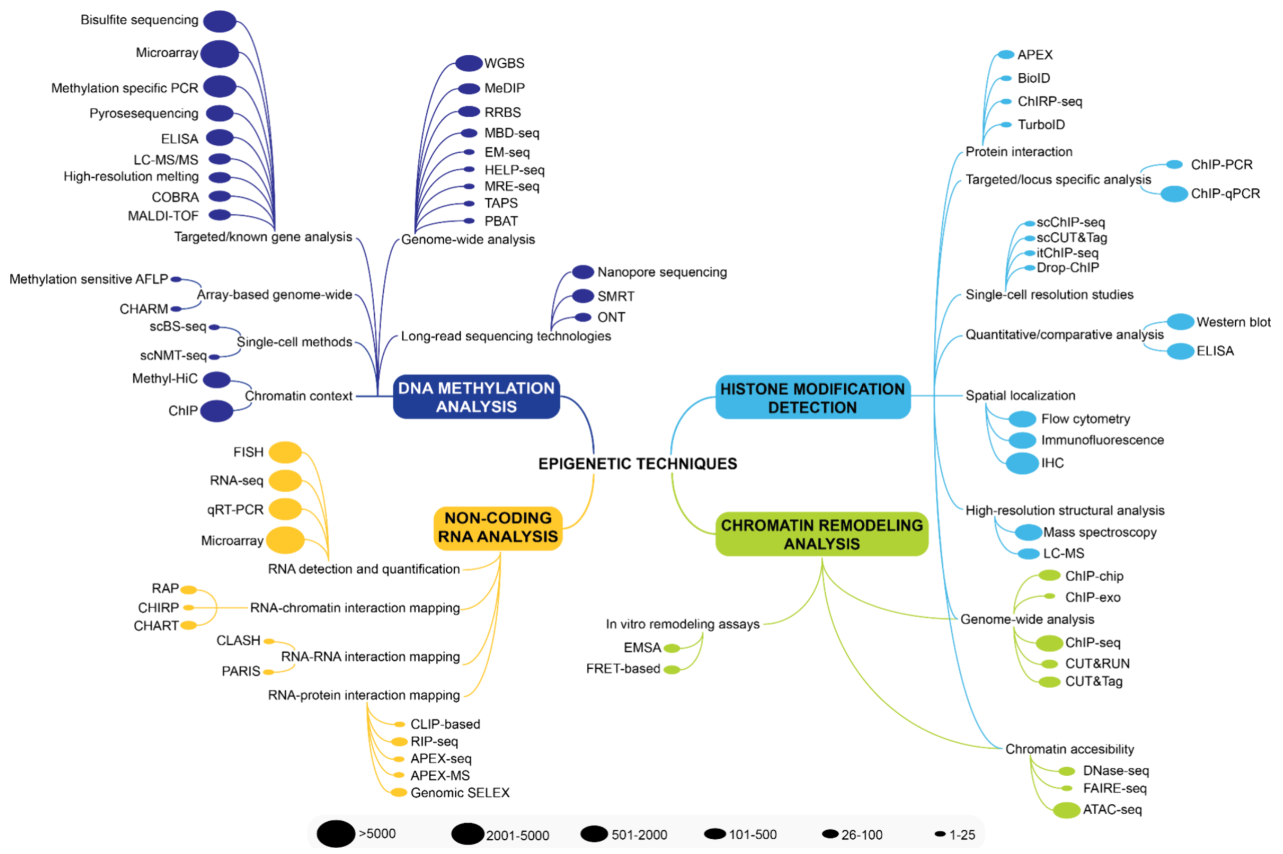
エピジェネティクス研究を支える、実験技術の豊かなエコシステムが存在し、それは主に以下の4つの主要なカテゴリーに分けられます:DNAメチル化解析(ビスアルファイトシーケンシング、メチル化アレイ)、ヒストン修飾検出(ChIP-seq、CUT&RUN)、ノンコーディングRNA解析(RNA-seq、CLIP-seq)、そしてクロマチンリモデリングプロファイリング(ATAC-seq、DNase-seq)。次世代のアプローチであるCUT&Tag、空間ATAC-seq、そしてロングリードナノポアシーケンシングなどが、研究の地平をさらに広げています。
エピゲノムプロファイリングと臨床データの統合は、精密医療のアプローチを可能にしています。Pharmacoepigenomicsは、薬剤の選択を支援します。例えば、MGMTのメチル化状態は、グリオブラスト患者がテモゾロマイドから恩恵を受けるかどうかを決定します。循環性エピジェネティックマーカーを用いたリキッドバイオプシーは、非侵襲的なモニタリングを提供します。AIと機械学習は、バイオマーカーの発見とエピジェネティックパターンの認識を加速させています。
Pharmacoepigenomics は、ファーマコゲノミクスのエピジェネティック的な側面です。ファーマコゲノミクスが遺伝的変異に基づいて薬剤の選択を誘導するのに対し、ファーマコエピジェノミクスはエピジェネティックなプロファイルを利用します。エピジェネティックなマーカーは、環境やライフスタイルによって動的に変化し、影響を受けるため、静的な遺伝的変異だけでは得られない、より具体的でタイムリーな情報を提供し、治療判断に役立ちます。
ライフスタイルや環境への曝露を明らかにする可能性のあるエピジェネティックデータのプライバシー。家族構成員に関する情報が明らかになる可能性のあるエピジェネティック検査におけるインフォームド・コンセントの課題。エピジェネティックプロファイルに基づく差別リスク。生殖細胞系列のエピジェネティック編集とその世代間への影響に関する倫理的な懸念。
エピジェネティック治療、特に生殖細胞系列の改変を規制するガイドラインの必要性が高まっています。エピジェネティックな改変や診断テストに関する知的財産権の考慮事項。データ保護法は、遺伝的素因と環境要因の履歴の両方を反映する、エピジェネティック情報の特有の機密性に対応するために進化する必要があります。
環境正義:汚染物質への曝露は、不利な立場にあるコミュニティに不均衡な影響を与え、世代を超えたエピジェネティックな影響をもたらします。有害な環境曝露を防ぐ責任が、新たな重要性を帯びてきます。エピジェネティクスと遺伝学を区別し、決定論的な誤解を避けるために、国民への教育が必要です。
AIを活用したエピゲノム解析によるパターン認識。DNAおよびRNAの直接的な修飾を検出するためのロングリードシーケンシング(ナノポア、PacBio)。エピゲノミクス、トランスクリプトミクス、プロテオミクスを組み合わせたマルチオミクス統合。高分解能なシングルセルおよび空間解析技術の向上。
がん治療にとどまらず、代謝性疾患、神経疾患、および炎症性疾患など、治療領域を拡大。エピ遺伝学関連薬剤(epi-drugs)と免疫療法、および標的分子に作用する薬剤を組み合わせた併用療法を開発。組織特異的およびアイソフォーム選択的な阻害剤を開発し、標的以外の部位への影響を低減。
エピジェネティックなマーキングの機能的検証:因果関係と相関関係の変化を区別する。エピジェネティックなメカニズム間の相互作用の理解。発生および疾患における、エピジェネティックな状態がどのように確立され、維持され、除去されるかの解明。
m6Aによって広範囲に修飾されるlncRNAは、その安定性と機能に影響を与えます。RNAの修飾パターンは、新たな診断バイオマーカーとなりえます。エピトランスクリプトーム機構を標的とする低分子阻害剤。包括的な治療戦略を理解するために、DNAとRNAの修飾間の相互作用を把握することが重要です。
急速な進歩にもかかわらず、依然として重要な課題が残されています:(1) 単一細胞の空間分解能を達成するための技術的な限界。(2) 遺伝子系列エピジェネティック編集に関する倫理的な懸念。(3) エピジェネティック、遺伝子、環境の相互作用の複雑さ。(4) 細胞の種類や組織における再現性の問題。(5) 薬剤耐性およびオフターゲット効果。(6) 標準化されたバイオマーカー検証プロトコルの必要性。
エピジェネティクス研究の分野は、目覚ましい変革を遂げ、分子生物学の専門分野から、人間の健康に深く影響を与える主要な生物医学分野へと発展しました。
このレビューでは、エピジェネティクス、分子生物学、臨床試験、および医薬品開発に関する600件以上の参考文献が引用されています。完全な参考文献リストについては、PMCに掲載されている原本をご参照ください。